题目内容
4.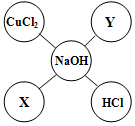 画知识结构图有助于我们认清知识间的联系.某同学在学习了氢氧化钠的性质后,画出了如图所示的化学性质关系图(“-”表示相连的两种物质能发生反应,五个圈中的物质分别属于不同的类别).
画知识结构图有助于我们认清知识间的联系.某同学在学习了氢氧化钠的性质后,画出了如图所示的化学性质关系图(“-”表示相连的两种物质能发生反应,五个圈中的物质分别属于不同的类别).(1)已知X是一种指示剂,则X可以是无色酚酞.(填一种即可)
(2)若Y是空气成分中物质,请写出氢氧化钠与Y反应的化学方程式:CO2+2NaOH═Na2CO3+H2O.
分析 根据碱的化学性质:碱能与非金属氧化物、酸、盐等反应进行分析解答.
解答 解:(1)氢氧化钠溶液能使无色酚酞试液变红,故填:无色酚酞;
(2)氢氧化钠能与二氧化碳反应生成碳酸钠和水,反应方程式是CO2+2NaOH═Na2CO3+H2O,故填:CO2+2NaOH═Na2CO3+H2O.
点评 本题难度不大,掌握碱的化学性质以及化学方程式的书写方法并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
15.某科学兴趣小组对石灰石样品和盐酸反应进行如下研究
①称取25.0克石灰石样品,平均分成两份,并分别加工成块状和粉末状
②将块状和粉末状的两份样品分别投入甲、乙两个锥形瓶中,同时加入足量的相同溶质质量分数的稀盐酸(样品所含杂质不溶于水也不与盐酸反应),测得锥形瓶总质量与反应时间的关系如表所示.请回答:
(1)由表格分析得出,影响该化学反应速率的因素是反应物的接触面积.
(2)充分反应后,每份样品生成二氧化碳的质量为4.4克.
(3)计算该样品中碳酸钙的质量分数.
①称取25.0克石灰石样品,平均分成两份,并分别加工成块状和粉末状
②将块状和粉末状的两份样品分别投入甲、乙两个锥形瓶中,同时加入足量的相同溶质质量分数的稀盐酸(样品所含杂质不溶于水也不与盐酸反应),测得锥形瓶总质量与反应时间的关系如表所示.请回答:
| 类型/时间 | 0 | 2分钟 | 4分钟 | 6分钟 | 8分钟 | 10分钟 | 12分钟 | 14分钟 |
| 甲锥形瓶 | 112.5克 | 111.6克 | 110.7克 | 109.9克 | 109.1克 | 108.5克 | 108.1克 | 108.1克 |
| 乙锥形瓶 | 112.5克 | 110.4克 | 109.3克 | 108.6克 | 108.1克 | 108.1克 | 108.1克 | 108.1克 |
(2)充分反应后,每份样品生成二氧化碳的质量为4.4克.
(3)计算该样品中碳酸钙的质量分数.
19.铁会生锈、能被磁铁磁化,铁能导电、在加热到一定温度时能熔化.铁的以上性质中属于化学性质的是( )
| A. | 铁会生锈 | B. | 铁能被磁铁磁化 | ||
| C. | 铁能导电 | D. | 铁加热到一定温度时能熔化 |
5.甲同学为了区别氢氧化钠和氢氧化钙溶液,设计了如下四组实验方案.

(1)其中能达到实验目的是CD;
(2)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,
得到的混合溶液中一定有的溶质为氯化钠;
(3)滴入酚酞后溶液呈红色,说明溶液呈碱性.为了确定碱性溶液中的溶质成分,甲同学查阅资料,获悉氯化钡溶液呈中性,设计如下实验加以验证.请根据要求完成下列空白:

(1)其中能达到实验目的是CD;
(2)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,
得到的混合溶液中一定有的溶质为氯化钠;
(3)滴入酚酞后溶液呈红色,说明溶液呈碱性.为了确定碱性溶液中的溶质成分,甲同学查阅资料,获悉氯化钡溶液呈中性,设计如下实验加以验证.请根据要求完成下列空白:
| 实验内容 | 预测现象 | 结论 |
| 取少量容器中的上层溶液于试管中,加入过量的氯化钡溶液,静置 | ①若有白色沉淀,溶液呈无色 | 物质是碳酸钠 |
| ②若无白色沉淀,溶液呈红色 | 物质是氢氧化钙,或氢氧化钠,或氢氧化钙和氢氧化钠 | |
| ③若有白色沉淀,溶液呈红色 | 物质是碳酸钠和氢氧化钠 |