��Ŀ����
9��2011 �� 9 �£��й���ҽ�о�Ա���������ֲ���ȡ�������أ���ѧʽΪC15H22O5�����������ŵ�����������֮��������˹�˽��������ֵ���������������ű����������������ߵ�������2015��10��5�յ���俨����ҽѧԺ5����������2015��ŵ��������ѧ��ҽѧ�������й�ҩѧ���������Լ���������ѧ������•���������ձ���ѧ�Ҵ���ǣ����������ڼ����漲�������о�����ȡ�õijɾͣ���1�����й��������ص�������ȷ���Ǣ٢ڢݣ�
�������������������
���������� C��H��O ����Ԫ�����
���������� 15 ��̼ԭ�ӡ�22 ����ԭ�Ӻ�5 ����ԭ�ӹ���
���������� C��H��O ����Ԫ�ص�������Ϊ 15��22��5
�������ص���Է�������Ϊ 282
��2���ӿ��ƴ�Ⱦ�����е��������ڿ��ǣ�����ű�����߷��������ء����ڿ��ƴ�ȾԴ��
��3��19 ��������������������Ⱥ���Ϊ����ű������Чҩ������������űԭ������˿�ҩ�ԣ�����Ч��Խ��Խ�����ҩ���űԭ����ж���ѡ��Ľ����Ҳ������Ի�����һ����Ӧ����
���� ��1�����ݺ���̼Ԫ�صĻ�������л�����������ػ�ѧʽ�ĺ��塢��Է�������Ϊ��ɷ��ӵĸ�ԭ�ӵ����ԭ������֮�͡��������и�Ԫ��������=��ԭ�ӵ����ԭ��������ԭ�Ӹ���֮�ȣ����з������
��2�����ݿ��ƴ�Ⱦ�����е��������ڽ��з����жϣ�
��3���������⡢���������Ӧ�Եĸ�����з������
��� �⣺��1���������أ���ѧʽΪC15H22O5���Ǻ�̼Ԫ�صĻ���������л��������ѡ��˵����ȷ��
���������أ���ѧʽΪC15H22O5����ѧʽ��֪������������C��H��O����Ԫ����ɣ���ѡ��˵����ȷ��
�����������������ط��ӹ��ɵģ��������أ���ѧʽΪC15H22O5����ѧʽ��֪��һ�������ط�������15��̼ԭ�ӡ�22����ԭ�Ӻ�5����ԭ�ӹ��ɣ���ѡ��˵������
����������C��H��O����Ԫ�ص�������Ϊ��12��15������1��22������16��5����15��22��5����ѡ��˵������
�������ص���Է�������Ϊ12��15+1��22+16��5=282����ѡ��˵����ȷ��
��2�����ƴ�Ⱦ�����е����������ǿ��ƴ�ȾԴ�����ƴ���;������������Ⱥ���Բ����緢�֡�����ϡ�����롢���������ڿ��ƴ�ȾԴ���ʡ���ű�����߷��������ء����ڿ��ƴ�ȾԴ��
��3��������Ӧ����ָ�ڽ��������У�����Ի����ı����Ӧ���������⣬űԭ������˿�ҩ�ԣ�����Ч��Խ��Խ�����ҩ���űԭ����ж���ѡ��Ľ����Ҳ������Ի�����һ����Ӧ����
�ʴ�Ϊ����1���٢ڢݣ���2�����ƴ�ȾԴ����3����Ӧ��
���� �����ѶȲ��������л����ѧʽ�ĺ��弰�йؼ��㡢���ƴ�Ⱦ�����е��������ڡ�������Ӧ�Եȼ�����ȷ����⣮

| A�� | 2Fe+3H2SO4�TFe2��SO4��3+3H2�� | B�� | H2SO4+Cu��OH��2�TCuSO4��+2H2O | ||
| C�� | Cu+2HCl�TCuCl2+H2�� | D�� | AgNO3+NaCl�TAgCl��+NaNO3 |
| A�� | ��� | B�� | ��ˮ | C�� | ֲ���� | D�� | ţ�� |
| A�� | Ũ�������ǿ��ʴ�ԣ�����Ũ������Һ��û��H+ | |
| B�� | Ũ�����Ũ���ᶼ������ˮ�� | |
| C�� | Ũ�������Ϊ����������Ը���CO��H2 | |
| D�� | ��ˮ����Ũ����ϡ�ͻ��ͷų��������� |
ij��ȤС��ͬѧ��NaOH��Na2CO3��NaHCO3��NaCl�ȳ������ƵĻ�����������о���
��֪ʶ�عˡ��������˵����ȷ����____��
A�����������������ռ�����ڸ����������� B��̼�����׳ƴ�����ڼ�
C��̼�������׳��մ���������θ����� D���Ȼ�������Ȼ������Ҫ�����ں�ˮ��
��������⡿NaOH¶���ڿ������ױ��ʣ���ôʵ�����е�����������û�б����أ���С��ͬѧ��ʵ������һƿ�������ƹ�����Ʒ�ijɷֽ�����̽����
���������ϡ���NaOH�ڿ����в���ת����NaHCO3��
��BaCl2��Һ�����ԣ�Ba(OH)2�ǿ����Լ
��CO2�ڱ��͵�NaHCO3��Һ�м������ܽ⡣
��������롿����٣���Ʒ��ֻ��NaOH
����ڣ���Ʒ��ֻ��Na2CO3
����ۣ���Ʒ�м���NaOH����Na2CO3
NaOH���ʷ�Ӧ�Ļ�ѧ����ʽΪ______________________��
��ʵ��̽������ȤС��ͬѧ�������ʵ�����̽����
ʵ����� | ʵ����������� |
1.ȡ������Ʒ��������ˮ�� | ��Ʒȫ���ܽ⣬����ɫ��Һ�� |
2.ȡ����ʵ��1������ɫ��Һ���Թ��У��μ�����ϡ���ᡣ | �����ݲ����������_____����١������ڡ��ۡ����������� |
3.ȡ����ʵ��1������ɫ��Һ���Թ��У��μ� ________��Һ�� | �а�ɫ�����������йػ�ѧ����ʽΪ________�� |
4.����һ��ʱ���ȡʵ��3���Թ����ϲ���Һ���μ� _______�� | ��Ӧ����____ �������۳����� |
�������о���������Ʒ���ʵij̶�����أ�����ȤС��ͬѧ�����ͼװ�òⶨ��Ʒ��Na2CO3������������

�������£�
�ٰ�ͼ���Ӻ�װ�ã�����������ԣ�
��ȷ��ȡ����Ʒ1.0g��������ƿ�ڣ�
�۴�Һ©���������μ�30.0%��ϡ�������������رջ�����
�ܷ�Ӧ��������Ͳ��Һ��Ķ���Ϊ55.0mL������֪�����������£�CO2���ܶ�Ϊ1.6g•L��1��
�� Bװ�ü���ƿ��ԭ�еĿ�����ʵ����____����С���û�С���Ӱ�졣)
�� B�м���ƿʢװ�ı��͵�̼��������Һ������ˮ���棬��������___________________��
�� ��ַ�Ӧ��װ��A�в����Ķ�����̼��ʵ�����Ƿ�������Ӱ�죿____����С���û�С���
�� �������Ʒ��Na2CO3����������______��д��������̣����������0.1%����
��ȥ���и������л��е��������ʣ������Լ��Ͳ�������ȷ����
��� | ���� | ���� | �����Լ��Ͳ������� |
A | CaCO3 | CaO | ���³������ |
B | H2 | HCl | ����ͨ��������NaOH��Һ��Ũ���� |
C | NaCl���� | ϸɳ | ��������ˮ�ܽ⡢���� |
D | ���� | Fe2O3 | ����������ϡ���ᣬ���ˡ�ϴ�ӡ����� |
A. A B. B C. C D. D
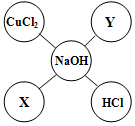 ��֪ʶ�ṹͼ��������������֪ʶ�����ϵ��ijͬѧ��ѧϰ���������Ƶ����ʺ�������ͼ��ʾ�Ļ�ѧ���ʹ�ϵͼ����-����ʾ���������������ܷ�����Ӧ�����Ȧ�е����ʷֱ����ڲ�ͬ����𣩣�
��֪ʶ�ṹͼ��������������֪ʶ�����ϵ��ijͬѧ��ѧϰ���������Ƶ����ʺ�������ͼ��ʾ�Ļ�ѧ���ʹ�ϵͼ����-����ʾ���������������ܷ�����Ӧ�����Ȧ�е����ʷֱ����ڲ�ͬ����𣩣�