题目内容
4.在宏观、微观和符号之间建立联系是化学学科的特点,对物质进行分类是化学研究的重要方法.现有物质①纯碱; ②锌粒;③硝酸钾;④氧化铝;⑤尿素,请按要求填写:由原子直接构成的是Zn(填写化学式),属于氧化物的是Al2O3(填写化学式),属于盐的是①③(填写序号),可用作化学肥料的是③⑤(填写序号).分析 根据金属、大多数固态非金属单质、稀有气体等由原子构成;氧化物是只含有两种元素且其中一种元素是氧元素的化合物;盐是由金属离子(或铵根离子)和酸根离子组成的化合物;含有氮元素的肥料称为氮肥,含有磷元素的肥料称为磷肥,含有钾元素的肥料称为钾肥,同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥;据此进行分析解答.
解答 解:锌粒属于金属单质,是由锌原子直接构成的,锌的化学式为Zn.
氧化铝是由铝元素和氧元素两种元素组成的,且有一种是氧元素的化合物,属于氧化物,铝元素显+3价,氧元素下-2价,其化学式为:Al2O3.
纯碱是碳酸钠的俗称,硝酸钾,纯碱、硝酸钾均是由金属离子和酸根离子组成的化合物,均属于盐.
硝酸钾中含有钾元素和氮元素,属于复合肥;尿素中含有氮元素,属于氮肥.
故答案为:Zn;Al2O3;①③;③⑤.
点评 本题难度不大,掌握由原子直接构成的物质(金属、大多数固态非金属单质、稀有气体等)、氧化物与盐的特征、化肥的分类方法是正确解答本题的关键.

练习册系列答案
相关题目
14.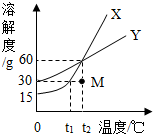 X、Y两种固体(均不带结晶水)物质的溶解度曲线如图所示,下列有关叙述错误的是( )
X、Y两种固体(均不带结晶水)物质的溶解度曲线如图所示,下列有关叙述错误的是( )
 X、Y两种固体(均不带结晶水)物质的溶解度曲线如图所示,下列有关叙述错误的是( )
X、Y两种固体(均不带结晶水)物质的溶解度曲线如图所示,下列有关叙述错误的是( )| A. | X、Y两种固体物质都是易溶性物质 | |
| B. | 降温t2℃X和Y的两杯饱和溶液到t1℃,析出的X一定比Y多 | |
| C. | 向M点65g X溶液中加入15g X固体能得到t2℃X的饱和溶液 | |
| D. | 降温(远高于t2℃)的X和Y的饱和溶液降温至0℃可初步提纯X |
15.下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )
| A. | Fe | B. | O2 | C. | N | D. | H2O |
19.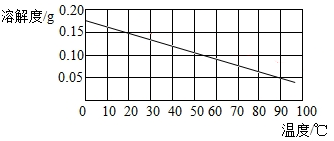 如图是氢氧化钙的溶解度曲线.30℃时,将1g氢氧化钙粉末加入到100g水中,充分搅拌后静置.下列说法你认为正确的是( )
如图是氢氧化钙的溶解度曲线.30℃时,将1g氢氧化钙粉末加入到100g水中,充分搅拌后静置.下列说法你认为正确的是( )
 如图是氢氧化钙的溶解度曲线.30℃时,将1g氢氧化钙粉末加入到100g水中,充分搅拌后静置.下列说法你认为正确的是( )
如图是氢氧化钙的溶解度曲线.30℃时,将1g氢氧化钙粉末加入到100g水中,充分搅拌后静置.下列说法你认为正确的是( )| A. | 所得溶液的质量为101g | B. | 所得溶液是不饱和溶液 | ||
| C. | 降低温度溶液的质量变大 | D. | 升高温度溶质质量分数变大 |
16.根据如图装置图回答问题.
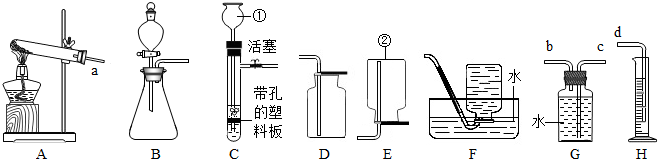
(1)实验室用一定质量的氯酸钾制取氧气,通过排水量测定所收集到的氧气体积.
①写出该反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
②各装置的连接顺序是:abcd.(用管口字母表示)
(2)某化学探究小组用HCl与大理石反应研究影响反应剧烈程度的因素.实验温度为25℃、35℃;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙60%的大理石10g;所用HCl的质量分数为9.125%、18.25%,每次实验HCl的用量为20mL(假设9.125%、18.25%的盐酸的密度均为1g/cm3;大理石中杂质不与盐酸反应).
【提出问题】:影响HCl与大理石反应的剧烈程度的因素有哪些?
【做出猜想】:
猜想一:大理石规格;猜想二:所用HCl溶液的质量分数;猜想三:实验温度.
【实验设计与实施】:完成以下实验设计方案并实验.
【实验结论】:在其他条件不变时,盐酸溶液质量分数越大,反应越剧烈;温度越高,反应越剧烈;固体的颗粒越小,反应越剧烈..

(1)实验室用一定质量的氯酸钾制取氧气,通过排水量测定所收集到的氧气体积.
①写出该反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
②各装置的连接顺序是:abcd.(用管口字母表示)
(2)某化学探究小组用HCl与大理石反应研究影响反应剧烈程度的因素.实验温度为25℃、35℃;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙60%的大理石10g;所用HCl的质量分数为9.125%、18.25%,每次实验HCl的用量为20mL(假设9.125%、18.25%的盐酸的密度均为1g/cm3;大理石中杂质不与盐酸反应).
【提出问题】:影响HCl与大理石反应的剧烈程度的因素有哪些?
【做出猜想】:
猜想一:大理石规格;猜想二:所用HCl溶液的质量分数;猜想三:实验温度.
【实验设计与实施】:完成以下实验设计方案并实验.
| 实验 编号 | T/℃ | 大理石 规格 | HCl的 质量分数 | 完全反应 的时间/s | 实验目的 |
| ① | 25 | 粗颗粒 | 18.25% | 160 | (Ⅰ)实验①和②探究同体积下HCl质量分数对该反应剧烈程度的影响. (Ⅱ)实验①和③探究温度对该反应剧烈程度的影响. (Ⅲ)实验①和④探究大理石规格对该反应剧烈程度的影响. |
| ② | 210 | ||||
| ③ | 35 | 粗颗粒 | 18.25% | 60 | |
| ④ | 100 |
13.下列有关分子、原子、离子的说法正确的是( )
| A. | 保持氧气化学性质的最小微粒是氧原子 | |
| B. | 原子的核外层电子数决定元素的种类 | |
| C. | 氯化钠是由离子构成的化合物 | |
| D. | 分子间有一定间隔,原子间没有间隔 |
14. 钚(Pu)是一种稀土元素,该元素在周期表中的信息如图所示,下列有关说法错误的是( )
钚(Pu)是一种稀土元素,该元素在周期表中的信息如图所示,下列有关说法错误的是( )
 钚(Pu)是一种稀土元素,该元素在周期表中的信息如图所示,下列有关说法错误的是( )
钚(Pu)是一种稀土元素,该元素在周期表中的信息如图所示,下列有关说法错误的是( )| A. | 钚是金属元素 | B. | 钚原子的质子数为94 | ||
| C. | 钚元素的相对原子质量为224 | D. | 钚原子的中子数为94 |
 如图是某保健品标签的部分内容,请仔细阅读后回答下列问题
如图是某保健品标签的部分内容,请仔细阅读后回答下列问题