题目内容
7.回答下列与水有关的问题.(1)活性炭能除去水中的异味和有色杂质,因为活性炭具有吸附性;
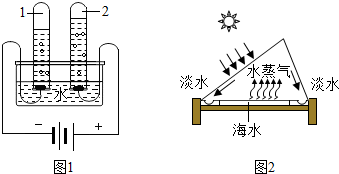
(2)电解水的实验中,只生成了氢气和氧气,说明水是由氢、氧元素组成的;
(3)水受热变成水蒸气的过程,水发生了物理变化(选填“物理变化”或“化学变化”);
(4)向某水样中滴加肥皂水搅拌,产生大量浮渣,该水样是硬水还是软水?硬水.
分析 (1)根据活性炭具有吸附性,能吸附异味和色素,进行分析解答.
(2)电解水生成氢气和氧气,说明水是由氢、氧两种元素组成的解答;
(3)根据是否生成新物质来分析;
(4)根据软水和硬水的鉴别方法考虑.
解答 解:(1)活性炭具有吸附性,能吸附异味和色素.故填:吸附;
(2)电解水生成氢气和氧气,说明水是由氢、氧两种元素组成的.故填:氢、氧元素;
(3)水受热变成水蒸气的过程中只是水的状态发生改变,没有新物质生成,属于物理变化.故填:物理变化.
(4)用肥皂水可以鉴别硬水和软水,泡沫多的是软水,浮渣较多,泡沫少的是硬水.故答案为:硬水.
点评 本题考查水的组成和构成,学生熟悉水的化学式的意义及物质类别的判断即可解答,难点是硬水中的成分及鉴别.

练习册系列答案
相关题目
18.在一个密闭容器中有X、Y、Z、Q四种物质,一定条件下充分反应,测得反应前后各物质的质量如表所示:
己知X和Q两种物质的相对分子质量均为M,下列推理中正确的足( )
| X | Y | Z | Q | |
| 反应前的质量/g | 8 | 10 | 1 | 21 |
| 反应后的质量/g | 0 | 21 | 待测 | 9 |
| A. | 反应后物质Z的质量为9g | |
| B. | 反应生成Y的质量为llg | |
| C. | 反应中物质Y与Q发生改变的质量之比为1:1 | |
| D. | 该反应的化学方程式中,物质X与Q的化学计量数之比为1:1 |
15.铁丝在氧气里燃烧后剩下来的球状物质中的成分是Fe3O4和少量铁,不含Fe2O3、Fe3O4和Fe2O3的分解温度,铁的熔点见表:下列有关说法错误的是( )
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | / |
| 熔点/℃ | / | / | 1535 |
| A. | 铁丝在氧气里燃烧时产生火星四射现象 | |
| B. | 可以用稀盐酸验证球状物质中含有铁 | |
| C. | 铁丝燃烧时温度高于1400℃而低于1535℃ | |
| D. | Fe3O4中铁元素具有两种化合价 |