题目内容
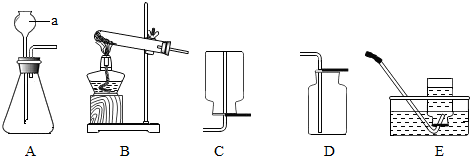
12.根据如图甲实验装置图,回答有关问题.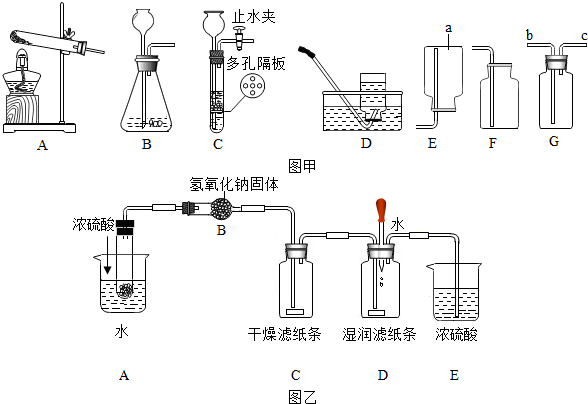
(1)装置图中仪器a的名称为集气瓶.
(2)用氯酸钾和二氧化锰混合共热制取氧气,可选用的装置组合是AD或AF,写出发生反应的化学方程式2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑.若改用高锰酸钾制取氧气,发生装置应作的改动是在试管口放一小团棉花.
(3)实验室利用B装置制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O,如果利用G装置收集二氧化碳,气体应从b 端通入(填“b”或“c”),用C装置代替B装置作为发生装置,其主要优点是随时控制反应的开始与停止,控制反应速率.
(4)某学生想要通过碳酸氢铵分解产生的氨气来探究氨水具有碱性,而氨气不具有碱性,按如图乙所示进行实验:(滤纸条用酚酞试液浸泡并晾干)
[资料]NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑ 2NH3+H2SO4═(NH4)2 SO4
试分析:A装置中加入浓硫酸的作用是浓硫酸溶于水放热,提供热量,B中氢氧化钠固体的作用是:Ⅰ.干燥气体;Ⅱ.CO2+2NaOH=Na2CO3+H2O(用化学方程式表示),该同学看到干燥的滤纸条不变红,湿润的滤纸条变红现象,得出了正确的结论.
分析 (1)熟记仪器的名称;
(2)实验室用氯酸钾和二氧化锰混合制取氧气,属于固体加热型,故应选用的发生装置是B,并写出反应方程式,高锰酸钾制取氧气应在试管口放一团棉花,防止加热时高锰酸钾粉末进入导管;
(3)根据实验室制取二氧化碳的原理、二氧化碳的性质来分析;
(4)浓硫酸溶于水放热,因此向A烧杯中加浓硫酸的作用是放热使NH4HCO3分解;氢氧化钠固体既吸收水蒸气,又吸收二氧化碳;干燥的氨气不具有碱性,石蕊试纸不变色;氨气溶于水生成氨水,D瓶中石蕊试纸变蓝色;E烧杯中稀硫酸的作用是:吸收氨气,防止氨气污染空气.
解答 解:(1)仪器a是集气瓶,故填:集气瓶;
(2)实验室用氯酸钾和二氧化锰混合制取氧气,属于固体加热型,故应选用的发生装置是A,反应方程式是:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,氧气的密度比空气大,不易溶于水,可用排水法或向上排空气法来收集;高锰酸钾制取氧气应在试管口放一团棉花,防止加热时高锰酸钾粉末进入导管;故填:AD或AF;2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;在试管口放一小团棉花;
(3)二氧化碳的实验室制法是用稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应来制取.其反应原理是CaCO3+2HCl=CaCl2+CO2↑+H2O;因二氧化碳的密度比空气大,如用G装置收集CO2,则气体应从b端入;用C装置代替B装置作为发生装置,能随时控制反应的开始与停止,控制反应速率;故填:CaCO3+2HCl=CaCl2+CO2↑+H2O;b;随时控制反应的开始与停止,控制反应速率;
(4)浓硫酸溶于水放热,因此向A烧杯中加浓硫酸的作用是放热使NH4HCO3分解;氢氧化钠固体既吸收水蒸气,又吸收二氧化碳;干燥的氨气不具有碱性,石蕊试纸不变色;氨气溶于水生成氨水,D瓶中石蕊试纸变蓝色;故填:浓硫酸溶于水放热,提供热量;CO2+2NaOH=Na2CO3+H2O;干燥的滤纸条不变红,湿润的滤纸条变红.
点评 本题考查知识比较综合,掌握实验室制取氧气的反应原理、发生和收集装置的选取方法,并能据装置特点分析其优越性,能较好考查学生分析和解决问题的能力.

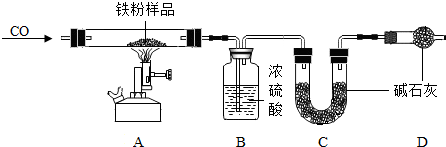
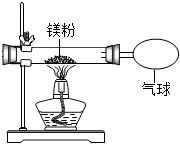 某兴趣小组甲为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组甲为验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
(2)实验中发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律.我不同意该小组的观点,因为空气中的氧气参加了反应;
(3)小组乙按如图装置改进实验,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【査阅资料】①氧化镁为白色固体:
②镁能与氮气剧烈反应生成黄色的氮化镁(MgN2)固体:③氮化镁可与水剧烈反应产生氨气.氨气极易溶于水,溶液呈碱性.
【做出猜想】黄色固体是MgN2
【实验探究】请设计实验,验证猜想:
| 实验操作 | 实验现象及结论 |
| 1 取少量黄色固体于试管中,加入适量的水 ②滴加酚酞试液 | 现象:①产生有刺激性气味的气体 ②酚酞试液变红色 结论:证明猜想正确 |
| A. | 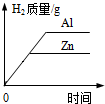 等物质的量且大小相同的锌片、铝片分别与足量且质量分数相同的稀硫酸反应 | |
| B. |  一定量锌片放入硫酸亚铁溶液中 | |
| C. | 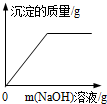 向CuCl2和HCl的混合溶液中滴加NaOH溶液 | |
| D. |  向饱和的硫酸铜溶液中加入硫酸铜粉末 |
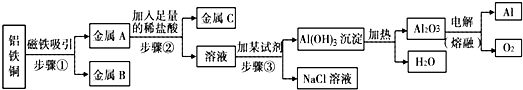
 已知A-G均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应,B是赤铁矿的主要成分,F为紫红色,E可用于配制农药波尔多液.根据如图所示的转化关系(图中反应条件均已略去),请回答:
已知A-G均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应,B是赤铁矿的主要成分,F为紫红色,E可用于配制农药波尔多液.根据如图所示的转化关系(图中反应条件均已略去),请回答: