题目内容
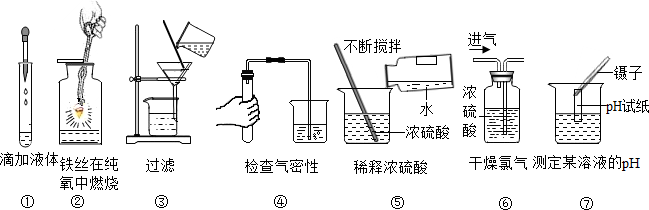
10.有些晶体按比例带有一定量的结晶水,带有结晶水的晶体在一定温度下会脱去结晶水.草酸晶体(H2C2O4•xH2O)在常温下是一种无色透明晶体.草酸晶体受热时分解的化学方程式为H2C2O4•xH2O═(x+1)H2O+CO2↑+CO↑某化学兴趣小组的同学利用该信息以及所学的知识设计并开展实验,测定草酸晶体中结晶水的质量分数.(图中固定装置已略去,装置气密性良好,装置A、B中的试剂足量,注射器量程足够)

Ⅰ.测量装置A、B的质量,排尽注射器中的空气,连接装置;
Ⅱ.取质量为m的草酸晶体,加热至完全分解,将产物全部通入以上装置;
Ⅲ.测量并记录装置A增加的质量为a,装置B增加的质量为b,装置C读数为V;
Ⅳ.甲乙丙三位同学分别利用装置ABC所得数据计算该草酸晶体中结晶水的质量分数
请回答下列问题:
(1)装置A中盛放的液体是浓硫酸;装置B的作用是吸收二氧化碳;装置C的作用之一是测量一氧化碳的体积.
(2)乙同学对利用装置B测量结果计算的可靠性进行反思与评价,认为反应后装置A中残留的气体会使自己的计算结果偏大(填“偏小”或“偏大”).
(3)甲同学依据装置A测量结果计算结晶水的质量分数为$\frac{100a}{m}$%(用代数式表示).
分析 (1)浓硫酸具有吸水性,可以用作氢气、氧气、二氧化碳等气体的干燥剂;
氢氧化钠溶液能够吸收二氧化碳气体;
一氧化碳不能和硫酸、氢氧化钠反应,不溶于水;
(2)反应后装置A中残留的气体中含有二氧化碳气体;
(3)结晶水的质量分数=$\frac{结晶水质量}{草酸晶体质量}$×100%.
解答 解:(1)装置A中盛放的液体是浓硫酸,用来吸收反应生成的水蒸气;
装置B的作用是吸收反应生成的二氧化碳气体;
装置C的作用之一是测量一氧化碳的体积.
故填:浓硫酸;吸收二氧化碳;一氧化碳.
(2)反应后装置A中残留有二氧化碳气体,会导致测定的二氧化碳质量偏小,从而导致计算结果偏大.
故填:偏大.
(3)甲同学依据装置A测量结果计算结晶水的质量分数为:$\frac{a}{m}$×100%=$\frac{100a}{m}$%.
故填:$\frac{100a}{m}$%.
点评 A、B中的浓硫酸和氢氧化钠溶液顺序不能颠倒,这是因为如果A中是氢氧化钠溶液,则进入浓硫酸中的水蒸气的量不一定是反应生成的水蒸气的量.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
3.下列各组物质能在pH=1的无色溶液中大量共存的是( )
| A. | NaCl、NaNO3、KNO3、(NH4)2SO4 | B. | H2SO4、HCl、AgNO3、Na2SO4 | ||
| C. | KMnO4、CuCl2、Fe2(SO4)3、NaNO3 | D. | K2SO4、NaCl、K2CO3、NaOH |
2.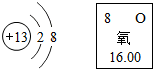 元素化合物知识是初中化学重要的学习内容.请回答下列有关元素化合物的问题.
元素化合物知识是初中化学重要的学习内容.请回答下列有关元素化合物的问题.
(1)根据如图信息,写出甲、乙两种元素的单质间发生反应的化学方程式:4Al+3O2=2Al2O3.
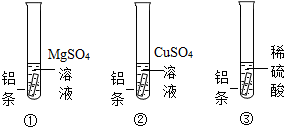
(2)某同学将铁片放入CuSO4溶液中,发现铁片表面有红色物质析出,同时还有少量无色无味气泡产生.对于产生气泡的“异常现象”,下列猜想不合理的是B(填字母).
A、产生的气体可能是H2 B、产生的气体可能是CO2
C、CuSO4溶液中可能含有少量的某种酸 D、CuSO4溶液的pH可能小于7
(3)某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方程式:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑),这种工业称为“氯碱工业”,某研究性学习小组对该厂生产的烧碱样品进行如下探究.
【提出问题】烧碱样品中含有哪些杂质?
【猜想】
猜想一:可能含有Na2CO3,作出此猜想的依据是:CO2+2NaOH=Na2CO3+H2O(用化学方程式表示).
猜想二:可能含有NaCl,作出此猜想的依据是:可能有少量的氯化钠没有反应(用简洁的文字表述).
【设计实验】
(4)某同学取100g含有H2SO4的酸性废水,然后滴加烧碱溶液中和,至溶液pH=7时,共消耗质量分数为20%的烧碱溶液20g.求这种废水中含H2SO4的质量分数.
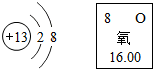 元素化合物知识是初中化学重要的学习内容.请回答下列有关元素化合物的问题.
元素化合物知识是初中化学重要的学习内容.请回答下列有关元素化合物的问题.(1)根据如图信息,写出甲、乙两种元素的单质间发生反应的化学方程式:4Al+3O2=2Al2O3.
(2)某同学将铁片放入CuSO4溶液中,发现铁片表面有红色物质析出,同时还有少量无色无味气泡产生.对于产生气泡的“异常现象”,下列猜想不合理的是B(填字母).
A、产生的气体可能是H2 B、产生的气体可能是CO2
C、CuSO4溶液中可能含有少量的某种酸 D、CuSO4溶液的pH可能小于7
(3)某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方程式:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑),这种工业称为“氯碱工业”,某研究性学习小组对该厂生产的烧碱样品进行如下探究.
【提出问题】烧碱样品中含有哪些杂质?
【猜想】
猜想一:可能含有Na2CO3,作出此猜想的依据是:CO2+2NaOH=Na2CO3+H2O(用化学方程式表示).
猜想二:可能含有NaCl,作出此猜想的依据是:可能有少量的氯化钠没有反应(用简洁的文字表述).
【设计实验】
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁 | 试管外壁发热 | 原因是氢氧化钠固体溶于水放热 |
| ②向①所得的溶液中逐渐加入稀硝酸至过量 | 一开始无明显现象,一段时间后产生能使澄清石灰水变浑浊的气体 | 样品中含有的杂质是碳酸钠 |
| ③向②所得的溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还含有的杂质是氯化钠 |
19. 小明设计了一个趣味喷泉实验装置(如图),其气密性良好.但实验时,当将A中的固体和液体混合后,B中尖嘴导管处并没有有“喷泉”产生.请你分析:A中加入的固体和液体可能是( )
小明设计了一个趣味喷泉实验装置(如图),其气密性良好.但实验时,当将A中的固体和液体混合后,B中尖嘴导管处并没有有“喷泉”产生.请你分析:A中加入的固体和液体可能是( )
 小明设计了一个趣味喷泉实验装置(如图),其气密性良好.但实验时,当将A中的固体和液体混合后,B中尖嘴导管处并没有有“喷泉”产生.请你分析:A中加入的固体和液体可能是( )
小明设计了一个趣味喷泉实验装置(如图),其气密性良好.但实验时,当将A中的固体和液体混合后,B中尖嘴导管处并没有有“喷泉”产生.请你分析:A中加入的固体和液体可能是( )| A. | 碳酸钠和盐酸 | B. | 氯化钡和稀硫酸 | ||
| C. | 二氧化锰和过氧化氢溶液 | D. | 锌粉和稀硫酸 |