题目内容
4.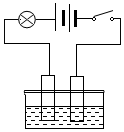 如图所示,烧杯中装有蒸馏水,
如图所示,烧杯中装有蒸馏水,(1)灯泡不发光(填发光或不发光)
(2)在烧杯中加入一定量的硫酸溶液后,灯泡发光(填发光或不发光)
(3)在(2)的前提下,逐渐滴加氢氧化钡溶液直至完全反应,在此过程中,灯泡的亮度将变暗.
分析 (1)根据物质的导电性来分析;
(2)根据酸的构成情况来分析;
(3)根据氢氧化钡与硫酸的反应分析回答.
解答 解:(1)蒸馏水没有导电性,灯泡不发光;故填:不发光;
(2)在烧杯中加入一定量的硫酸溶液后,溶液中存在着大量的能够自由移动的氢离子与硫酸根离子,灯泡 发光,故填:发光;
(3)稀硫酸中存在着大量的能够自由移动的氢离子与硫酸根离子,所以导电性较强,灯泡很亮,硫酸与氢氧化钡反应生成硫酸钡沉淀和水,因此随着Ba(OH)2溶液的滴加,硫酸减少,而生成的水不导电,硫酸钡是不溶于水的沉淀,溶液中可以自由移动的离子减少,溶液的导电能力变弱,流过灯泡的电流变小,灯泡变暗至熄灭,故填:变暗.
点评 此题是一道跨学科的题目,解题的关键是知道溶液导电的原因,以及化学反应对离子浓度的影响.

练习册系列答案
相关题目
4.分类法、类比分析法都是学习化学获取知识的重要科学方法.
(1)给定下列物质:H2、O2、CH4、CuO、CO2、CO对上述物质进行平均分成两类.其中一类是H2、CO、CH4;分类的依据是是否具有可燃性;
(2)比较比H2、CO、CH4均可作燃料,其中最理想的燃料是H2;比较还原性时,假设CH4有还原性,请写出在加热的条件下与CuO反应的化学方程式CH4+4CuO$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4Cu+2H2O.
(1)给定下列物质:H2、O2、CH4、CuO、CO2、CO对上述物质进行平均分成两类.其中一类是H2、CO、CH4;分类的依据是是否具有可燃性;
(2)比较比H2、CO、CH4均可作燃料,其中最理想的燃料是H2;比较还原性时,假设CH4有还原性,请写出在加热的条件下与CuO反应的化学方程式CH4+4CuO$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4Cu+2H2O.
| H2 | CO | CH4 | |
| 可燃性 | 有 | 有 | 有 |
| 还原性 | 有 | 有 | ? |
11.除去下列物质中的少量杂质,所选试剂及操作都正确的是( )
| 序号 | 物质 | 杂质 | 试剂 | 操作 |
| A | FeCl2溶液 | CuCl2 | 过量铁粉 | 结晶 |
| B | NH3(气) | H2O(气) | 浓硫酸 | 洗气 |
| C | NaNO3溶液 | Na2CO3 | 适量CaCl2溶液 | 过滤 |
| D | 铜粉 | 锌粉 | 过量盐酸 | 过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
16.现有铁、铜、银三种金属,限用一种试剂一次性就可验证他们的金属活动性强弱,则该试剂是( )
| A. | FeSO4溶液 | B. | 稀硫酸 | C. | AgNO3溶液 | D. | CuSO4溶液 |
 氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ Cl2↑+H2↑+2NaOH.现取一定质量的溶质质量分数为10%的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电.生成氯气的质量与反应时间的关系如图所示.
氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ Cl2↑+H2↑+2NaOH.现取一定质量的溶质质量分数为10%的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电.生成氯气的质量与反应时间的关系如图所示.