题目内容
17.火药是我国古代四大发明之一,火药由硫磺、硝石、木炭三种物质按一定质量比混合而成,请回答下列问题:(1)火药属于混合物(填“纯净物”或“混合物”)
(2)已知某种配比的火药,在空气中燃烧的化学方程式如下:S+2KNO3+3C=K2S+X↑+3CO2↑,则X的化学式为N2.
(3)硫磺的主要成分为硫,硫在空气中燃烧产生淡蓝色火焰,其生成的二氧化硫是形成酸雨的主要物质(填“酸雨”或“臭氧空洞”)
(4)木炭是我国古代用作燃料的物质,其充分燃烧生成二氧化碳,试写出检验二氧化碳的化学方程式是Ca(OH)2+CO2=CaCO3↓+H2O.
分析 (1)纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质,据此结合黑火药的成分进行分析解答;
(2)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式;
(3)硫粉在空气中燃烧,产生微弱的淡蓝色火焰,其生成的二氧化硫是形成酸雨的主要物质;
(4)检验二氧化碳气体用澄清的石灰水.
解答 解:(1)火药由硫磺、硝石、木炭三种物质按一定质量比混合而成,属于混合物;
(2)在反应2KNO3+S+3C═K2S+X+3CO2↑中,根据质量守恒定律可知,反应前后的元素种类、原子的种类和个数不变,K、S、C、O原子的个数在反应前后相等;反应前有N元素,则X中含有N元素,反应前共2个N原子,则反应后共有2个N原子,又X的化学计量数为1,则X的化学式为N2;
(3)硫粉在空气中燃烧,产生微弱的淡蓝色火焰,其生成的二氧化硫是形成酸雨的主要物质;
(4)检验二氧化碳气体用澄清的石灰水,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.
故答案为:(1)混合物;(2)N2;(3)淡蓝色;酸雨;(4)Ca(OH)2+CO2=CaCO3↓+H2O.
点评 本题难度不大,主要考查质量守恒定律的应用和化学方程式的书写等,可依据已有的知识解答.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
7.从海水中制取粗盐的方法是把海水引入盐田,经过风吹日晒使海水中的水分蒸发获得粗盐,在盐田中( )
| A. | 氯化钠的质量分数变小 | B. | 氯化钠的质量分数始终不变 | ||
| C. | 氯化钠的质量不变 | D. | 水的质量不变 |
8.某元素R的氧化物RxOy,式量为M,则R元素的相对原子质量是( )
| A. | $\frac{M-16y}{y}$ | B. | $\frac{M-16y}{x}$ | C. | M-16y | D. | $\frac{16x-M}{x}$ |
6.下列物质属于纯净物的是( )
| A. | 可口可乐 | B. | 纯净的空气 | C. | 啤酒 | D. | 干冰 |
3.下列实验现象描述正确的是( )
| A. | 把氢氧化镁加入到无色的酚酞试液中,试液变成红色 | |
| B. | 打开浓盐酸的试剂瓶的瓶盖,瓶口会有白雾出现 | |
| C. | 氧化铁和稀硫酸反应,最后得到浅绿色溶液 | |
| D. | 铜片放入硝酸银溶液中,溶液会由蓝色逐渐变为无色 |
 手机早已成为老百姓不可或缺的物品之一,而很多人喜欢给心爱的手机加一个外壳,既为了保护,也能彰显个性.手机壳不仅外观多样,其材质也是五花八门,主要有塑料、硅胶、金属、皮革等.
手机早已成为老百姓不可或缺的物品之一,而很多人喜欢给心爱的手机加一个外壳,既为了保护,也能彰显个性.手机壳不仅外观多样,其材质也是五花八门,主要有塑料、硅胶、金属、皮革等. 有A、B、C、D、E、F、G七种不同化合物,它们有如图所示的反应关系(图中的“-”表示相连两物质之间可以发生反应,图中的“→”表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物已略去).已知:B和D,C和E,F和G分别为相同类型的物质;A是胃酸的主要成分,F为红色固体.请写出:
有A、B、C、D、E、F、G七种不同化合物,它们有如图所示的反应关系(图中的“-”表示相连两物质之间可以发生反应,图中的“→”表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物已略去).已知:B和D,C和E,F和G分别为相同类型的物质;A是胃酸的主要成分,F为红色固体.请写出: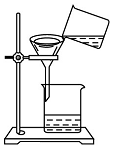 小红同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问:
小红同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问: