题目内容
11.为得到纯净的物质,某同学设计下表中的除杂方法,其中方法正确的是( )| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CaCl2 | HCl | 加入过量CaCO3,过滤 |
| B | H2SO4 | HNO3 | 加入适量BaCl2溶液,过滤 |
| C | O2 | N2气体 | 将气体缓缓通过灼热的铜网 |
| D | Na2SO4溶液 | CuSO4 | 加入过量氢氧化钠溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、HCl能与过量的碳酸钙反应生成氯化钙、水和二氧化碳,再过滤除去过量的碳酸钙,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、H2SO4能与适量BaCl2溶液反应生成硫酸钡沉淀和盐酸,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、O2通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、CuSO4能与过量氢氧化钠溶液反应生成氢氧化铜沉淀和硫酸钠,能除去杂质但引入了新的杂质氢氧化钠(过量的),不符合除杂原则,故选项所采取的方法错误.
故选:A.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
1.下列由事实得出的结论正确的是( )
| 编号 | 事实 | 结论 |
| A | 某溶液能使紫色石蕊溶液显红色 | 该溶液一定是酸溶液 |
| B | 给固体加热时试管破裂 | 试管口肯定没有略向下倾斜 |
| C | 某物质由多种元素组成 | 该物质一定不是单质 |
| D | 某物质与酸反应产生大量气泡 | 该物质一定是活泼金属 |
| A. | A | B. | B | C. | C | D. | D |
2.某固体由FeSO4和Fe2(SO4)3混合而成的,经测定其中硫的质量分数为a,则铁的质量分数是( )
| A. | 1-a | B. | 1-2a | C. | 1-2.5a | D. | 1-3a |
16.如表是市场上销售的一种常见氮肥的包装说明书.请阅读有关内容后,回答下列问题:
(1)NH4Cl和K2SO4都是可作化学肥料的物质.虽然它们没有共同的组成元素,但在物质的分类中它们同属于盐类.
(2)化学肥料通常所说的“含氮量”中的“氮”是指元素.
| 主要成分 | NH4Cl |
| 保存方法 | 干燥阴凉处存放 |
| 含氮量 | ≥25% |
(2)化学肥料通常所说的“含氮量”中的“氮”是指元素.
3. 某同学为了探索物质的性质,以氧气为例,做了如下实验:
某同学为了探索物质的性质,以氧气为例,做了如下实验:
如图所示先收集了一瓶氧气(注意:瓶口向上)后正放在桌上,盖好玻璃片,然后用带火星的木条插入集气瓶,木条复燃从实验可以说明氧气的性质是( )
 某同学为了探索物质的性质,以氧气为例,做了如下实验:
某同学为了探索物质的性质,以氧气为例,做了如下实验:如图所示先收集了一瓶氧气(注意:瓶口向上)后正放在桌上,盖好玻璃片,然后用带火星的木条插入集气瓶,木条复燃从实验可以说明氧气的性质是( )
| A. | 氧气密度比空气小 | B. | 氧气可以燃烧 | ||
| C. | 氧气能供给呼吸 | D. | 氧气能支持燃烧 |

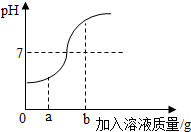 (1)该反应的化学方程式为:H2SO4+2NaOH=Na2SO4+2H2O.
(1)该反应的化学方程式为:H2SO4+2NaOH=Na2SO4+2H2O.