题目内容
1.课后,小明取氢氧化钠溶液,滴加氯化钙溶液后,有白色浑浊出现,为什么?分析 根据氢氧化钠与氯化钙溶液交换成分没有沉淀、气体或水生成,不能发生反应;氢氧化钠溶液能与空气中的二氧化碳反应生成碳酸钠,碳酸钠能与氯化钙反应生成碳酸钙白色沉淀,进行分析解答.
解答 解:氢氧化钠与氯化钙溶液交换成分没有沉淀、气体或水生成,不能发生反应;氢氧化钠溶液能与空气中的二氧化碳反应生成碳酸钠,碳酸钠能与氯化钙反应生成碳酸钙白色沉淀,故小明取氢氧化钠溶液,滴加氯化钙溶液后,有白色浑浊出现.
故答案为:氢氧化钠溶液变质后生成的碳酸钠溶液与氯化钙溶液反应生成碳酸钙白色沉淀.
点评 本题难度不大,掌握氢氧化钠的化学性质、碳酸钠的化学性质并能灵活运用是正确解答本题的关键.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
11.下列实验操作正确的是( )
| A. |  | B. |  | ||
| C. | 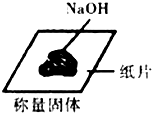 | D. | 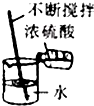 |
12.实验室处理一批过期的化学药品,兴趣小组同学决定对一瓶已经结块的氢氧化钠样品展开探究,请你参与.【探究活动一】证明变质的样品仍然有氢氧化钠存在
资料摘要:碳酸钠的水溶液呈碱性,氯化钠、氯化钙的水溶液呈中性.
(1)氢氧化钠暴露在空气中发生变质反应的化学方程式为CO2+2NaOH=Na2CO3+H2O.
同学们按照如下所示的步骤进行实验:
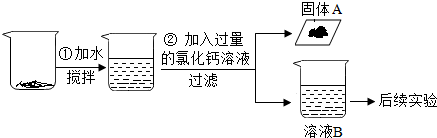
(2)步骤②中加入过量的氯化钙溶液的目的是除去碳酸钠,避免对氢氧化钠的验证产生干扰; 固体 A 必定含有的物质是CaCO3(写化学式).
(3)“后续实验”验证氢氧化钠的存在,请你简述实验步骤和产生的现象:向滤液B中滴加2-3滴酚酞试液,无色变红色,说明有氢氧化钠
【探究活动二】测定样品中碳酸钠的质量分数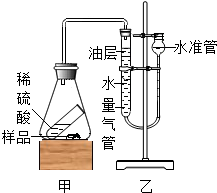
取 5.3g 样品与足量的稀硫酸反应,测量生成二氧化碳的体积,从而计算出碳酸钠的质量分数.实验装置如图(不考虑其他因素的影响,装置的气密性良好):
(4)倾斜锥形瓶使样品与稀硫酸充分接触.写出甲装置中发生反应的一个化学方程式:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
(5)量气管中水面上要加一层植物油(二氧化碳 不溶于该油层),目的是防止二氧化碳溶于水并与水反应
(6)实验测得的部分数据如下表所示:
根据表中的实验数据计算,反应生成的二氧化碳体积为220mL,已知在实验条件下,二氧化碳的密度为 2g•L-1,则生成二氧化碳的质量为0.44g
(7)通过计算,样品中碳酸钠的质量分数为20%.
资料摘要:碳酸钠的水溶液呈碱性,氯化钠、氯化钙的水溶液呈中性.
(1)氢氧化钠暴露在空气中发生变质反应的化学方程式为CO2+2NaOH=Na2CO3+H2O.
同学们按照如下所示的步骤进行实验:

(2)步骤②中加入过量的氯化钙溶液的目的是除去碳酸钠,避免对氢氧化钠的验证产生干扰; 固体 A 必定含有的物质是CaCO3(写化学式).
(3)“后续实验”验证氢氧化钠的存在,请你简述实验步骤和产生的现象:向滤液B中滴加2-3滴酚酞试液,无色变红色,说明有氢氧化钠
【探究活动二】测定样品中碳酸钠的质量分数

取 5.3g 样品与足量的稀硫酸反应,测量生成二氧化碳的体积,从而计算出碳酸钠的质量分数.实验装置如图(不考虑其他因素的影响,装置的气密性良好):
(4)倾斜锥形瓶使样品与稀硫酸充分接触.写出甲装置中发生反应的一个化学方程式:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
(5)量气管中水面上要加一层植物油(二氧化碳 不溶于该油层),目的是防止二氧化碳溶于水并与水反应
(6)实验测得的部分数据如下表所示:
| 反应前 | 反应后 | |
| 量气管内液面对应的刻度 | 42ML | 262mL |
(7)通过计算,样品中碳酸钠的质量分数为20%.
16.某水泥厂新进一批石灰石原料,该厂检验室为了测定该石灰石中碳酸钙的质量分数,取该样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸但也不溶于水)有关实验数据如表:(假设烧杯的质量为82g)
(1)反应中生成二氧化碳的质量为4.4g;
(2)求该石灰石中碳酸钙的质量分数(结果保留一位小数);
(3)反应后生成溶液的溶质的质量分数是多少?(结果保留一位小数)
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 152.0g | 12.0g | 159.6g | |
(2)求该石灰石中碳酸钙的质量分数(结果保留一位小数);
(3)反应后生成溶液的溶质的质量分数是多少?(结果保留一位小数)
16.人体缺乏下列哪种元素会导致甲状腺肿大( )
| A. | 钙 | B. | 碘 | C. | 氟 | D. | 锌 |
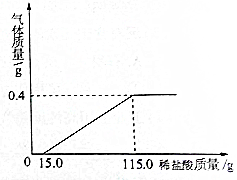 现有12.8g已生锈的铁片,将其放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如图所示(假设铁片除有铁锈外,不含其他杂质),回答:
现有12.8g已生锈的铁片,将其放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如图所示(假设铁片除有铁锈外,不含其他杂质),回答: 小明看到家里××牌钙片的说明书,部分文字说明如图所示,他对该钙片的含钙量有疑问,于是取出10片做探究实验.当加入50g溶质质量分数为7.3%的稀盐酸时,二者恰好完全反应.
小明看到家里××牌钙片的说明书,部分文字说明如图所示,他对该钙片的含钙量有疑问,于是取出10片做探究实验.当加入50g溶质质量分数为7.3%的稀盐酸时,二者恰好完全反应.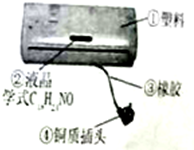 空调是常见的家用电器,如图为空调的实物图.
空调是常见的家用电器,如图为空调的实物图.