题目内容
10.化学与生活、生产密切相关.请回答:①家用净水器中使用活性炭是利用了它的吸附性;
②空气中氧气的体积百分含量是21%;
③最简单的有机物是CH4;(用化学式填空,下同)
④产生酸雨的主要物质是SO2;
⑤改良酸性土壤常用的物质是Ca(OH)2;
⑥生石灰是常见的食品干燥剂,请写出它与水反应的化学方程式CaO+H2O=Ca(OH)2.
分析 ①根据活性炭具有吸附性解答;
②根据空气中氧气的体积百分含量是21%解答;
③根据最简单的有机物是甲烷解答;
④根据产生酸雨的主要物质是二氧化硫解答;
⑤根据氢氧化钙常用于改良酸性土壤解答;
⑥根据生石灰具有吸水性解答.
解答 解:
①家用净水器中使用活性炭是利用了它的吸附性;
②空气中氧气的体积百分含量是21%;
③最简单的有机物是甲烷,化学式为:CH4
④产生酸雨的主要物质是二氧化硫;
⑤氢氧化钙常用于改良酸性土壤;
⑥生石灰具有吸水性,它与水反应的化学方程式为:CaO+H2O=Ca(OH)2
答案:①吸附;②21%;③CH4;④SO2 ⑤Ca(OH)2 ⑥CaO+H2O=Ca(OH)2
点评 本题考查的是常见的物质的用途,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
相关题目
18.氧化镁在医药、建筑等行业应用广泛.以菱镁矿(主要成分为MgCO3,含少量FeCO3,其他杂质不溶于酸)为原料制备高纯氧化镁的实验流程如下:

(1)酸溶之前要将矿石粉碎的目的是增大接触面积,使反应更快更充分.稀硫酸需要过量的目的是将碳酸镁和碳酸亚铁完全反应.酸溶步骤中碳酸镁溶解的反应方程式为MgCO3+H2SO4═MgSO4+CO2↑+H2O,属于复分解反应(填反应基本类型).
(2)已知Mg2+、Fe2+和Fe3+在溶液中遇到氨水均可以转化成难溶性碱沉淀,开始沉淀和沉淀完全的pH如下表:
流程“氧化”一步中H2O2的作用是将溶液中的Fe2+转化成Fe3+,不能直接沉淀Fe2+的原因是防止Mg2+沉淀,此步骤中要控制温度不能太高,原因是防止过氧化氢分解.滤渣2的化学式是Fe(OH)3.

(1)酸溶之前要将矿石粉碎的目的是增大接触面积,使反应更快更充分.稀硫酸需要过量的目的是将碳酸镁和碳酸亚铁完全反应.酸溶步骤中碳酸镁溶解的反应方程式为MgCO3+H2SO4═MgSO4+CO2↑+H2O,属于复分解反应(填反应基本类型).
(2)已知Mg2+、Fe2+和Fe3+在溶液中遇到氨水均可以转化成难溶性碱沉淀,开始沉淀和沉淀完全的pH如下表:
| Mg2+ | Fe2+ | Fe3+ | |
| 开始沉淀 | 9.4 | 7.9 | 2.7 |
| 沉淀完全 | 12.4 | 9.6 | 3.7 |
5.有关物质的用途正确的是( )
| A. | 氢氧化钙用于治疗胃酸过多 | B. | 氧气用作火箭燃料 | ||
| C. | 胆矾用于检验水 | D. | 食盐溶液用于消毒杀菌 |
15.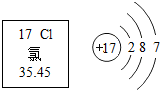 如图是氯元素在周期表中的相关信息和氯原子结构示意图.下列说法错误的是( )
如图是氯元素在周期表中的相关信息和氯原子结构示意图.下列说法错误的是( )
 如图是氯元素在周期表中的相关信息和氯原子结构示意图.下列说法错误的是( )
如图是氯元素在周期表中的相关信息和氯原子结构示意图.下列说法错误的是( )| A. | 氯原子核内的质子数是17 | B. | 氯原子核外有三个电子层 | ||
| C. | 氯元素的相对原子质量是35.45g | D. | 氯原子在化学反应中,易得到电子 |
9.去年我国多地出现雾霾天气现象,下列措施对PM2.5(直径小2.5μm的颗粒物)的治理不能起到枳极作用的是( )
| A. | 人力植树造林 | B. | 人力发展煤炭发电 | ||
| C. | 合理开发洁净能源 | D. | 禁止焚烧农作物秸秆和垃圾 |
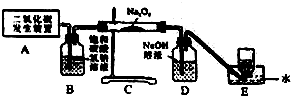 过氧化钠(Na2O2)是呼吸面具里产生氧气的原料,是一种淡黄色固体,能与CO2和H2O分别发生以下反应:
过氧化钠(Na2O2)是呼吸面具里产生氧气的原料,是一种淡黄色固体,能与CO2和H2O分别发生以下反应:
 溶解度是解决溶液相关问题的重要依据,请根据右图溶解度曲线解决下列问题(M、N均不含结晶水):
溶解度是解决溶液相关问题的重要依据,请根据右图溶解度曲线解决下列问题(M、N均不含结晶水):
