题目内容
20.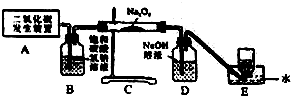 过氧化钠(Na2O2)是呼吸面具里产生氧气的原料,是一种淡黄色固体,能与CO2和H2O分别发生以下反应:
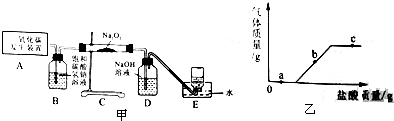
过氧化钠(Na2O2)是呼吸面具里产生氧气的原料,是一种淡黄色固体,能与CO2和H2O分别发生以下反应:2Na2O2+2CO2=2Na2CO3+O2;2Na2O2+2H2O=4NaOH+O2↑.某化学兴趣小组的同学在实验室中用下图所示装置制取二氧化碳并探究其与过氧化钠(Na2O2)的反应.
(1)装置B的作用是吸收CO2中混有的HCl,发生反应的化学方程式为NaHCO3+HCl═NaCl+H2O+CO2↑.装置D的作用是什么?
(2)为探究反应后装置C硬质玻璃管中固体的成分,该小组同学进行以下实验:Ⅰ.将固体溶于水,没有气泡产生;Ⅱ.然后向其中加入足量氯化钙溶液,有白色沉淀生成;Ⅲ.过滤后在滤液中滴加酚酞溶液,液体变为红色.
①反应后装置C硬质玻璃管中固体为碳酸钠和氢氧化钠.写出加入氯化钙溶液时发生反应的化学方程式.
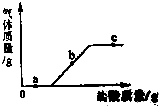
②取一定量步骤Ⅰ的溶液,逐滴滴加稀盐酸,根据实验情况绘制了右图.则a点发生反应的化学方程式为NaOH+HCl═NaCl+H2O;c点所示溶液中的溶质有哪些?
(3)若要证明二氧化碳能否与过氧化钠反应产生氧气,以上实验装置设计有不足之处,请写出改进的方法.
(4)实验室里制取8.8g二氧化碳,理论上需要质量分数为10%的稀盐酸的质量是多少?
分析 (1)碳酸氢钠能和稀盐酸反应生成氯化钠、水和二氧化碳;
氢氧化钠溶液能够吸收二氧化碳气体,并且氢氧化钠能和二氧化碳反应生成碳酸钠和水;
(2)碳酸钠能和氯化钙反应生成白色沉淀碳酸钙和氯化钠;
显碱性的溶液能使酚酞试液变红色;
稀盐酸和氢氧化钠反应生成氯化钠和水;
(3)氧气能使带火星的木条复燃;
(4)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳.
解答 解:(1)装置B的作用是吸收CO2中混有的HCl,稀盐酸能和碳酸氢钠反应生成氯化钠、水和二氧化碳,发生反应的化学方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑;
装置D的作用是吸收二氧化碳气体.
故答案为:NaHCO3+HCl═NaCl+H2O+CO2↑;吸收二氧化碳气体.
(2)Ⅰ.将固体溶于水,没有气泡产生;
Ⅱ.然后向其中加入足量氯化钙溶液,有白色沉淀生成,说明固体中含有碳酸钠;
Ⅲ.过滤后在滤液中滴加酚酞溶液,液体变为红色,说明固体中含有氢氧化钠;
①反应后装置C硬质玻璃管中固体为碳酸钠和氢氧化钠;
加入氯化钙溶液时发生反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl.
故答案为:碳酸钠和氢氧化钠;Na2CO3+CaCl2═CaCO3↓+2NaCl.
②a点时,稀盐酸和氢氧化钠反应生成氯化钠和水,发生反应的化学方程式为:NaOH+HCl═NaCl+H2O;
c点所示溶液中的溶质有反应生成的氯化钠和过量的氯化氢.
故答案为:NaOH+HCl═NaCl+H2O;氯化钠和氯化氢.
(3)改进的方法是:把排水法改为向上排空气法收集气体,并且把带火星的木条伸入集气瓶中,如果带火星的木条复燃,说明产生了氧气.
(4)设需要稀盐酸质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
73 44
x×10% 8.8g
$\frac{73}{x×10%}$=$\frac{44}{8.8g}$,
x=146g,
答:实验室里制取8.8g二氧化碳,理论上需要质量分数为10%的稀盐酸的质量是146g.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

| A. | 溶液中的溶质都是固体 | |
| B. | 溶液一定是无色透明的混合物 | |
| C. | 稀溶液可能是饱和溶液,浓溶液也可能是不饱和溶液 | |
| D. | 从一杯质量分数为10%的硝酸钾溶液中倒出一半,余下的溶液质量分数为5% |
| A. | 食盐,氧气 | |
| B. | 冰水混合物,铁丝 | |
| C. | 红磷,河水 | |
| D. | 净化后的空气,高锰酸钾加热完全分解后的固体剩余物 |
| A. | 蒸馏水 | B. | 加碘食盐 | C. | 食醋 | D. | 碳酸饮料 |
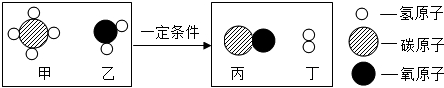
根据以上微观示意图得到的结论中,正确的是( )
| A. | 该反应是置换反应 | B. | 反应中氢元素有化合态变为游离态 | ||
| C. | 反应前后,分子、原子的种类均不变 | D. | 反应中丙丁分子数比为1:1 |