题目内容
9.丁丁在实验室发现一瓶未知浓度的氢氧化钠溶液,为方便以后使用,他对其浓度进行了测定.取20.0g此氢氧化钠溶液于烧杯中,逐滴滴加溶质质量分数为7.3%的稀盐酸,并随时对反应后的溶液用pH计(一种测定溶液pH的仪器)测定溶液的pH,所得数据如下表,试回答:| 加入稀盐酸的质量/g | 9.6 | 9.8 | 9.9 | 10.0 | 10.1 |
| 溶液的pH | 12.4 | 12.1 | 11.8 | 7.0 | 2.2 |
(2)请你替丁丁计算该氢氧化钠溶液溶质的质量分数.

(3)爱动脑筋的丁丁想:若取20.0g溶质质量分数为7.3%的稀盐酸,用该未知浓度的氢氧化钠溶液来逐滴滴加至完全反应,同样可测出氢氧化钠溶液溶质的质量分数.他还认为即便没有pH计,只要有无色酚酞也可粗略测定.你认
为他会选择如图的甲方式(选“甲”或“乙”)来测定.
分析 氢氧化钠和稀盐酸反应生成氯化钠和水.根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)当滴加稀盐酸的质量为10.1g时,溶液PH=2,说明稀盐酸过量,溶液中的溶质是NaCl、HCl.
故填:NaCl、HCl.
(2)设氢氧化钠质量为x,
NaOH+HCl═NaCl+H2O,
40 36.5
x 10.0g×7.3%
$\frac{40}{x}$=$\frac{36.5}{10.0g×7.3%}$,
x=0.8g,
该氢氧化钠溶液溶质的质量分数为:$\frac{0.8g}{20.0g}$×100%=4%,
答:该氢氧化钠溶液溶质的质量分数为4%.
(3)利用甲进行时,当溶液刚好由红色变成无色时,说明恰好完全反应,计算结果比较准确,利用乙进行时,当溶液由无色变成红色时,氢氧化钠过量,计算结果有误差,因此应该选择如图的甲方式来测定.
故填:甲.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
17.下列实验方案的设计中,没有正确体现对比这种科学思想的是( )
| A. | 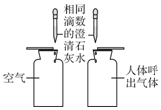 比较二氧化碳的含量 | B. | 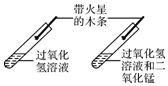 研究二氧化锰的催化作用 | ||
| C. | 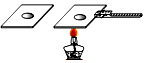 研究蒸发快慢影响的因素 | D. | 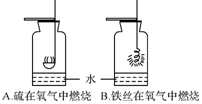 实验中水的作用 |
1.ClO2是一种黄绿色、有刺激性气味的气体,在食品保鲜、饮用水消毒等方面有广泛应用.下列有关ClO2说法正确的是( )
| A. | 在物质分类上属于盐类 | B. | 具刺激性气味是一种物理性质 | ||
| C. | 相对分子质量为67.5克 | D. | 该物质中氯元素的化合价为+1价 |
18.下列实验操作或装置正确的是( )
| A. | 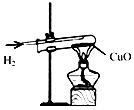 氢气还原氧化铜 氢气还原氧化铜 | B. | 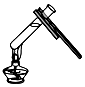 加热液体 | C. | 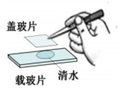 盖盖玻片 | D. |  使用测电笔 |
 .
. .
.