题目内容
2.根据元素周期表回答以下问题
(1)10号元素分类是稀有气体,16号元素的离子符号是S2-.
(2)写出12号元素与17号元素形成化合物的化学式MgCl2
(3)从表中找出一条规律元素周期表中,每个周期都是按原子序数递增的顺序进行排列的.
分析 (1)根据10号元素为氖元素,16号元素的最外层电子数为6,容易得到2个电子进行解答;
(2)根据12号元素与17号元素分别为镁元素和氯元素进行解答;
(3)根据表中信息进行解答.
解答 解:(1)10号元素为氖元素,属于稀有气体;16号元素的最外层电子数为6,容易得到2个电子,离子符号为S2-;故填:稀有气体;S2-;
(2)12号元素与17号元素分别为镁元素和氯元素,其中镁元素的化合价为+2价,氯元素的化合价为-1价,所以形成化合物的化学式MgCl2;故填:MgCl2;
(3)同一周期的元素是按原子序数递增的顺序进行排列的,故填:元素周期表中,每个周期都是按原子序数递增的顺序进行排列的.
点评 明确质子数决定元素种类,最外层电子数决定元素的化学性质,元素周期表是按照原子序数递增的顺序排列的,知道原子结构示意图中各部分含义.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
20.“水培”是一种室内植物无土栽培方式,又名“营养液培”.配制菠菜营养液时需要用到下列物质,其中属于复合肥料的是( )
| A. | H2O | B. | (NH4)2S04 | C. | KH2PO4 | D. | Ca(NO3)2 |
17.如图是物质A、B、C的溶解度曲线,下列相关说法正确的是( )
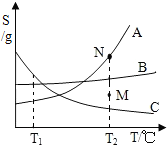

| A. | 若要将B从溶液中结晶出来常采用的方法是降温结晶 | |
| B. | 将T2℃时A、B、C的饱和溶液冷却到T1℃,A溶液的溶质质量分数最小 | |
| C. | 若要将组成在M点的A溶液转变为N点的溶液,只能采取恒温蒸发溶剂的方法 | |
| D. | 将T2℃时组成在M点的C与水的混合物降温至T1℃时,可能得到C的不饱和溶液 |
14.欲改变一杯饱和硝酸钾溶液的溶质质量分数,有以下方法:①升高温度 ②加少量水 ③加入少量硝酸钾 ④降低温度 ⑤恒温蒸发部分水.可行的方法是( )
| A. | ②④ | B. | ②③④⑤ | C. | ②④⑤ | D. | ①②④⑤ |
11. 如图是探究酵母菌呼吸作用的实验装置,下列叙述错误的是( )
如图是探究酵母菌呼吸作用的实验装置,下列叙述错误的是( )
 如图是探究酵母菌呼吸作用的实验装置,下列叙述错误的是( )
如图是探究酵母菌呼吸作用的实验装置,下列叙述错误的是( )| A. | ①中加NaOH是为了清除空气中CO2 | |
| B. | ②的葡萄糖是酵母菌呼吸作用的底物 | |
| C. | ②中酵母菌只能在有氧条件下生存 | |
| D. | ③中加Ca(OH)2用于检测②中是否有CO2产生 |
12.金属的应用与其性质密切相关.在“金属与盐溶液反应”的探究课上,同学们将硝酸银溶液倒入装有铜粉的试管中,充分反应后观察到的铜的表面析出银白色物质以及溶液由无色变成蓝色,发生反应的化学方程式为Cu+2AgNO3=Cu(NO3)2+2Ag.过滤后,得到滤渣和滤液.同学们进行了如下探究.
【提出问题】:滤液中溶质的成分是什么?
【猜想与假设】:猜想一:硝酸铜 猜想二:硝酸银和硝酸铜.
【进行实验】:
【解释与结论】:根据对滤液成分的分析,可以推断出滤渣可能的成分是②③(填序号,下同)
①铜 ②银 ③铜和银
【拓展与延伸】:对滤渣回收后,老师要求将滤液中较多的铜离子除去后再排放,以减少对环境的污染.同学们可以向滤液中加入适量的①③.
①铁 ②稀硫酸 ③氢氧化钠溶液 ④氧化钠溶液.
【提出问题】:滤液中溶质的成分是什么?
【猜想与假设】:猜想一:硝酸铜 猜想二:硝酸银和硝酸铜.
【进行实验】:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,向其中滴入稀盐酸 | 无明显现象 | 猜想一正确 |
①铜 ②银 ③铜和银
【拓展与延伸】:对滤渣回收后,老师要求将滤液中较多的铜离子除去后再排放,以减少对环境的污染.同学们可以向滤液中加入适量的①③.
①铁 ②稀硫酸 ③氢氧化钠溶液 ④氧化钠溶液.

