题目内容
9.以下是鉴别稀盐酸和碳酸钠溶液中其他相关的探究实验【进行实验】
| 序号 | 操作步骤 | 实验结论 | |
| 实验一 | 分别用A、B两支试管取样,然后各加入同一种指示剂溶液 | A中不变色; B中指示剂变红色 | B中物质是碳酸钠 |
| 实验二 | 分别用A、B两支试管取样,然后各加入足量的氢氧化钙溶液 | B中产生白色的沉淀 |
②实验二结束后A试管中一定存在离子有Ca2+(写离子符号)
【提出问题】实验二结束后B试管中的废液中含有的溶质成分是什么?
【提出猜想】猜想1:含有氢氧化钠.
猜想2:含有氢氧化钠和碳酸钠.
猜想3:含有氢氧化钠和氢氧化钙.
【实验探究】某同学用pH试纸测出废液的pH=10,判断猜想2成立.该判断不正确,原因是三种情况下的溶液均显碱性.该同学通过其他实验方法证明猜想2确实成立.
分析 【思考与分析】(1)根据酸碱指示剂的变色情况来分析;(2)根据氢氧化钙溶液与碳酸钠溶液反应的现象、稀盐酸与氢氧化钙反应的产物来分析;
【提出猜想】根据哪一种反应物可能剩余来分析;根据碳酸钠溶液和氢氧化钠、氢氧化钙溶液均显碱性来分析.
解答 解:【思考与分析】(1)无色酚酞试液遇到酸性溶液不变色,遇到碱性溶液变红色,
(2)氢氧化钙与碳酸钠反应生成碳酸钙白色沉淀;稀盐酸与氢氧化钙反应生成氯化钙和水,因为氢氧化钙足量,可能有剩余的氢氧化钙,
【提出猜想】氢氧化钙与碳酸钠有可能恰好完全反应,也有可能碳酸钠或氢氧化钙剩余;
氢氧化钙溶液、氢氧化钠溶液与碳酸钠溶液都显碱性,pH大于7.
故答案为:
| 序号 | 操作步骤 | 实验结论 | |
| 实验一 | 分别用A、B两支试管取样,然后各加入同一种指示剂溶液 | A中 不变色; B中指示剂变红色 | B中物质是碳酸钠 |
| 实验二 | 分别用A、B两支试管取样,然后各加入足量的氢氧化钙溶液 | B中 产生白色的沉淀 |
三种情况下的溶液均显碱性.
点评 掌握物质之间反应规律以及实验探究的设计方法是解题的关键.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
20.某密闭容器中有W、氧气和二氧化碳三种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表.根据表中信息,判断下列说法正确的是( )
| 物质 | W | O2 | CO2 | H2O |
| 反应前质量/g | 16 | 70 | 1 | 0 |
| 反应后质量/g | 0 | 待测 | 45 | 36 |
| A. | 该反应可能是氧化反应 | |
| B. | W中一定含有碳、氢两种元素,质量比为3:1 | |
| C. | W中一定含有碳、氢两种元素,可能含有氧 | |
| D. | 反应生成的CO2和H2O的质量比为45:36 |
1.下列实验操作正确的是( )
| A. | 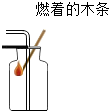 二氧化碳验满 | B. | 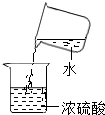 稀释浓硫酸 | C. |  给液体加热 | D. |  测溶液pH |



