题目内容
4.下列离子能在pH=1的水溶液中大量共存的是( )| A. | SO42-、NO3-、K+、OH- | B. | Cl-、SO42-、Na+、Ba2+ | ||
| C. | Cl-、NO3-、K+、Mg2+ | D. | Ca2+、Cl-、CO32-、K+ |
分析 pH为1的水溶液显酸性,水溶液中含有大量的H+.根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能大量共存;进行分析判断.
解答 解:pH为1的水溶液显酸性,水溶液中含有大量的H+.
A、氢离子和氢氧根离子结合生成水,故选项错误.
B、SO42-、Ba2+离子结合生成硫酸钡沉淀,故选项错误.
C、四者之间不反应,能在酸性溶液中共存,故选项正确.
D、氢离子和碳酸根离子结合生成水和二氧化碳,故选项错误.
故选:C.
点评 本题难度不大,考查物质的共存问题,判断物质在溶液中能否共存,主要看溶液中的各物质之间能否发生反应生成沉淀、气体、水.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案
相关题目
14.在硝酸银、硝酸铜、硝酸镁的混合溶液中加入一定量铁粉,反应停止后过滤,滤液仍为蓝色.有关判断正确的是( )
| A. | 滤渣中一定有银和铁,可能有铜 | |
| B. | 滤渣中一定有银,一定没有铜和铁 | |
| C. | 滤液中一定有硝酸镁、硝酸亚铁、硝酸铜、硝酸银 | |
| D. | 滤液中一定有硝酸镁、硝酸亚铁、硝酸铜、可能有硝酸银 |
16.在研究人体呼吸作用的课堂上,老师通过实验,让学生比较呼出的气体与吸入的空气中氧气和二氧化碳含量的变化情况.步骤如下表:
(1)检验二氧化碳的物质①是澄清的石灰水.
(2)现象②是石灰水立即变浑浊.
(3)分析现象得出:结果③是呼出的气体中氧气的含量比吸入的空气中少(多/少);结果④是呼出的气体中二氧化碳的含量比吸入的空气中多(多/少).
(4)根据以上分析,可以得出人体的生命活动消耗了氧气,释放了二氧化碳.
| 检验物质 | 检验方法 | 实验现象 | 实验结果 | |
| 吸入的空气 | 呼出的气体 | |||
| 氧气 | 将燃着的小木条伸入集气瓶 | 短时间内继续燃烧 | 立即熄灭 | ③ |
| 二氧化碳 | 将气体通入等量的① | 一段时间后变浑浊 | ② | ④ |
(2)现象②是石灰水立即变浑浊.
(3)分析现象得出:结果③是呼出的气体中氧气的含量比吸入的空气中少(多/少);结果④是呼出的气体中二氧化碳的含量比吸入的空气中多(多/少).
(4)根据以上分析,可以得出人体的生命活动消耗了氧气,释放了二氧化碳.
13. 目前世界上最精确的钟是以锶做钟摆的钟,锶的原子结构示意图及元素周期表中某些信息如图所示,下列说法正确的是( )
目前世界上最精确的钟是以锶做钟摆的钟,锶的原子结构示意图及元素周期表中某些信息如图所示,下列说法正确的是( )
 目前世界上最精确的钟是以锶做钟摆的钟,锶的原子结构示意图及元素周期表中某些信息如图所示,下列说法正确的是( )
目前世界上最精确的钟是以锶做钟摆的钟,锶的原子结构示意图及元素周期表中某些信息如图所示,下列说法正确的是( )| A. | x的值为8 | B. | 锶属于非金属元素 | ||
| C. | 锶的相对原子质量为87.62g | D. | 锶原子在化学反应中易失去电子 |
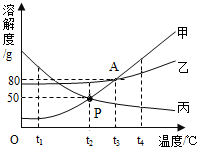 如图为甲、乙、丙三种物质的溶解度曲线.回答下列问题:
如图为甲、乙、丙三种物质的溶解度曲线.回答下列问题: A、B、C、D是初中化学常见的物质,各物质之间的相互转化的关系如图所示(部分反应物、生成物及条件略去).已知:四种物质均含有铜元素,且铜在化合物中均为+2价;A为单质,C溶液呈蓝色;D为不溶于水的蓝色固体.
A、B、C、D是初中化学常见的物质,各物质之间的相互转化的关系如图所示(部分反应物、生成物及条件略去).已知:四种物质均含有铜元素,且铜在化合物中均为+2价;A为单质,C溶液呈蓝色;D为不溶于水的蓝色固体.