题目内容
14.在硝酸银、硝酸铜、硝酸镁的混合溶液中加入一定量铁粉,反应停止后过滤,滤液仍为蓝色.有关判断正确的是( )| A. | 滤渣中一定有银和铁,可能有铜 | |
| B. | 滤渣中一定有银,一定没有铜和铁 | |
| C. | 滤液中一定有硝酸镁、硝酸亚铁、硝酸铜、硝酸银 | |
| D. | 滤液中一定有硝酸镁、硝酸亚铁、硝酸铜、可能有硝酸银 |
分析 根据四种金属活动性由强到弱的顺序:镁>铁>铜>银,当把铁粉加入到硝酸银、硝酸铜、硝酸镁的混合溶液中时,银首先被置换出来,在银完全置换后,铜才能被置换出来,硝酸镁不与铁粉反应;一定量的铁粉,可能完全转换出银,也可能只置换出部分的银,滤液呈蓝色,说明滤液中含有硝酸铜,铁可能没有置换出铜,有可能置换出部分铜等知识进行分析.
解答 解:A、铁会首先与硝酸银发生置换反应,所以滤渣中一定有银,铁可能与硝酸铜反应,有可能没有反应,所以滤渣中可能含有铜,由于有硝酸铜的剩余,则一定没有铁,故选项错误;
B、根据反应后的滤液显蓝色,说明滤渣中一定没有铁,否则会继续和硝酸铜反应,故选项错误;
C、铁和硝酸银发生了置换反应,溶液显蓝色,所以滤液中一定含有硝酸铜和硝酸亚铁;铁也可能反应了少量的硝酸银,也可能将硝酸银全部反应完,所以滤液中可能含有硝酸银,故选项错误;
D、铁和硝酸银发生了置换反应.溶液显蓝色,所以滤液中一定含有硝酸铜和硝酸亚铁;铁也可能反应了少量的硝酸银,也可能将硝酸银全部反应完,所以滤液中可能含有硝酸银,故选项正确.
故选:D.
点评 本题考查了金属活动性顺序的应用,金属放入盐的混合溶液中,总是把活动性最弱的金属最先置换完,再按由弱到强的顺序一一进行置换.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案
相关题目
5.下列实验操作错误的是( )
| A. | 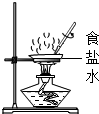 蒸发食盐水 | B. | 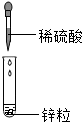 滴管的使用 | ||
| C. | 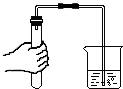 检查装置的气密性 | D. | 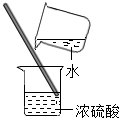 稀释浓硫酸 |
2. 甲、乙、丙、丁四种物质的相互反应关系如图所示(“一”表示相连的物质间能发生反应)下列符合对应反应关系的选项是( )
甲、乙、丙、丁四种物质的相互反应关系如图所示(“一”表示相连的物质间能发生反应)下列符合对应反应关系的选项是( )
 甲、乙、丙、丁四种物质的相互反应关系如图所示(“一”表示相连的物质间能发生反应)下列符合对应反应关系的选项是( )
甲、乙、丙、丁四种物质的相互反应关系如图所示(“一”表示相连的物质间能发生反应)下列符合对应反应关系的选项是( ) | 选项 | A | B | C | D | |
| 物 | 甲 | BaCl2 | CO2 | H2 | Fe |
| 乙 | Na2CO3 | NaOH | O2 | HCl | |
| 质 | 丙 | H2SO4 | CaCl2 | CuO | CuSO4 |
| 丁 | Ca(OH)2 | AgNO3 | CO | NaOH | |
| A. | A | B. | B | C. | C | D. | D |
19.下列物质长时间放置在空气中,质量增加且变质的是( )
| A. | 浓硫酸 | B. | 浓盐酸 | C. | 氢氧化钠固体 | D. | 碳酸钙 |
6.下列符号与其叙述对应一致的是( )
| A. | 3H--3个氢元素 | |
| B. | C60--60个碳原子 | |
| C. | ${\stackrel{+3}{AI}}_{\;}$2O3--氧化铝中铝元素的化合价为+3价 | |
| D. | NaCl2--氯化钠 |
4.下列离子能在pH=1的水溶液中大量共存的是( )
| A. | SO42-、NO3-、K+、OH- | B. | Cl-、SO42-、Na+、Ba2+ | ||
| C. | Cl-、NO3-、K+、Mg2+ | D. | Ca2+、Cl-、CO32-、K+ |