题目内容
3.下面是元素周期表中1-18号元素原子结构示意图的排列情况,通过你的学习,探究回答下列问题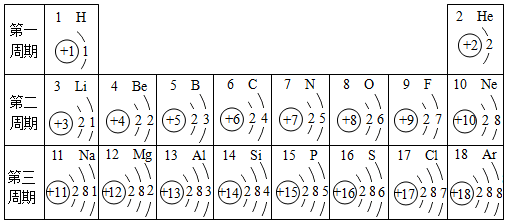
(1)13号元素在化学反应中容易失(填“得”或“失”)电子,变成Al3+(填写离子符号).
(2)写出8号元素与12号元素形成化合物的化学式MgO.
(3)经过你的观察,同一族(同一竖行)元素的原子最外层电子数相同,具有相似的化学性质.
(4)请你再观察,同一周期(同一横行)元素的原子具有电子层数相等规律.(写一条即可)
分析 最外层电子数小于4个的,反应中容易失去电子,大于4个的,反应中容易得到电子;
同一族中原子的最外层电子数相等,同一周期中原子的核外电子层数相等.
解答 解:(1)13号元素是铝元素,最外层电子数是3个,在化学反应中容易失电子,变成Al3+.
故填:失;Al3+.
(2)8号元素是氧元素,12号元素是镁元素,氧元素和镁元素形成化合物的化学式是MgO.
故填:MgO.
(3)同一族(同一竖行)元素的原子最外层电子数相同,具有相似的化学性质.
故填:最外层电子数;化学性质.
(4)同一周期(同一横行)元素的原子电子层数相等,最外层电子数依次递增等.
故填:电子层数相等.
点评 元素周期表反映了元素之间的内在联系,要注意理解和应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.一瓶气体经检验发现只含有一种元素,则这瓶气体是( )
| A. | 纯净物 | B. | 单质 | ||
| C. | 混合物 | D. | 可能是单质,也有可能是混合物 |
14.如图所示实验操作或设计正确的是( )
| A. |  倾倒液体药品 | B. |  铁丝的燃烧 | ||
| C. |  过滤河水 | D. |  向试管中滴加液体 |
8.工业用盐亚硝酸钠(NaNO2),不能食用.亚硝酸钠中氮元素的化合价为( )
| A. | -3 | B. | +1 | C. | +3 | D. | +5 |
12.下列现象或事实,用分子、原子的相关知识加以解释,其中不正确是( )
| 现象或事实 | 解释 | |
| A | 稀有气体可作保护气 | 构成它们的原子达到了稳定结构 |
| B | 敞口容器中的酒精逐渐减少 | 分子在不断的运动 |
| C | 水沸腾后壶盖被顶起 | 温度升高,分子体积变大 |
| D | 水通电分解 | 在化学变化分子可以再分 |
| A. | A | B. | B | C. | C | D. | D |
13.将锌、铁、镁、铝的混合粉末3.6g投入到一定质量的稀硫酸中,恰好完全反应后,得到200g含水88.6%的溶液,则得到氢气的质量是( )
| A. | 0.1 g | B. | 0.2 g | C. | 0.3 g | D. | 0.4 g |
