题目内容
10.粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙).某实验小组的同学在粗盐提纯实验中,并把少量可溶性杂质CaCl2,MgCl2一并除去,设计如下实验方案,请回答问题:
(1)实验操作A的名称是过滤;
(2)写出步骤③中发生反应的主要化学方程式MgCl2+2NaOH=Mg(OH)2↓+2NaCl;沉淀b中含有物质Mg(OH)2CaCO3(填化学式);
(3)实验中某同学对溶液b的成分进行了探究.
【提出问题】溶液b中除了含有水和氯化钠外,还含有哪些物质?
【提出猜想】根据实验①②③④⑤的操作后,作出如下猜想.
猜想一:还含有碳酸钠;
猜想二:还含有氢氧化钠;
猜想三:还含有碳酸钠和氢氧化钠.
【验证猜想】
| 步骤 | 实验操作 | 实验现象 | 推断 |
| 1 | 取少量溶液b于试管中,加入过量的氯化钙溶液,振荡,静置 | 产生白色沉淀 | 溶液b中还含有碳酸钠溶质 |
| 2 | 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入无色酚酞试液(填指示剂) | 溶液变红色 | 溶液b中还含有氢氧化钠 |
【反思与拓展】为了使制得的精盐水只含有水和氯化钠,步骤⑥的作用是除去杂质,请写出其中一个反应的化学方程式:HCl+NaOH=NaCl+H2O或2HCl+Na2CO3=2NaCl+H2O+CO2↑.
分析 (1)根据过滤可以将不溶性固体从溶液中分离进行分析;
(2)根据氢氧化钠和氯化镁反应会生成氢氧化镁沉淀和氯化钠,碳酸钠和氯化钙反应会生成碳酸钙沉淀和氯化钠进行分析;
(3)【验证猜想】根据碳酸钠和氯化钙反应会生成碳酸钙沉淀和氯化钠,酚酞遇碱变红色进行分析;
【实验结论】根据验证猜想的推断结果进行分析;
【反思与拓展】根据氢氧化钠和盐酸反应生成氯化钠和水,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳进行分析.
解答 解:(1)过滤可以将不溶性固体从溶液中分离,所以实验操作A的名称是过滤;
(2)氢氧化钠和氯化镁反应会生成氢氧化镁沉淀和氯化钠,碳酸钠和氯化钙反应会生成碳酸钙沉淀和氯化钠,所以步骤③中发生反应的主要化学方程式是:MgCl2+2NaOH=Mg(OH)2↓+2NaCl;沉淀b中含有物质是:Mg(OH)2、CaCO3;
(3)【验证猜想】碳酸钠和氯化钙反应会生成碳酸钙沉淀和氯化钠,酚酞遇碱变红色,所以
| 步骤 | 实验操作 | 实验现象 | 推断 |
| 1 | 取少量溶液b于试管中,加入过量的氯化钙溶液,振荡,静置 | 产生白色沉淀 | 溶液b中还含有碳酸钠溶质 |
| 2 | 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入无色酚酞试液(填指示剂) | 溶液变红色 | 溶液b中还含有氢氧化钠 |
【反思与拓展】氢氧化钠和盐酸反应生成氯化钠和水,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:HCl+NaOH=NaCl+H2O或2HCl+Na2CO3=2NaCl+H2O+CO2↑.
故答案为(1)过滤;
(2)MgCl2+2NaOH=Mg(OH)2↓+2NaCl,Mg(OH)2、CaCO3;
(3)【验证猜想】
| 步骤 | 实验操作 | 实验现象 | 推断 |
| 1 | 产生白色沉淀 | 溶液b中还含有碳酸钠(或Na2CO3)溶质 | |
| 2 | 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入无色酚酞试液 | 溶液变红色 | 溶液b中还含有氢氧化钠 |
【反思与拓展】HCl+NaOH=NaCl+H2O或2HCl+Na2CO3=2NaCl+H2O+CO2↑.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
3.下列叙述中,正确的是( )
| A. | 红磷在空气中燃烧产生大量白雾 | |
| B. | 人体缺少必需微量元素会得病,因此应尽可能多吃含有这些元素的营养补剂 | |
| C. | 电解水时加入氢氧化钠可增强导电性 | |
| D. | 吹灭蜡烛后的瞬间,烛芯处产生大量黑烟 |
3.厨房里发生的下列变化中,没有新物质生成的是( )
| A. | 煤气燃烧 | B. | 开水沸腾 | C. | 铁锅生锈 | D. | 蔬菜腐烂 |
15.滴管是初中科学实验中经常使用的仪器.下列各图中有关滴管的操作正确的是( )
| A. |  取液时挤入空气 | B. |  将滴管横放在桌面 | ||
| C. |  使用后未经冲洗直接放回原滴瓶 | D. | 将 残留试液的滴管倒持 |
19.今年以来,全国各地出现了几次较为严重的雾霾天气,再次引起人们对空气质量的关注,下列举措有利于改善空气质量的是( )
| A. | 露天焚烧垃圾 | B. | 燃煤火力发电 | ||
| C. | 鼓励开私家车出行 | D. | 工厂废气处理后排放 |
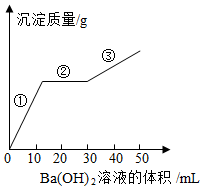 某溶液是由硫酸钠、碳酸钠、盐酸、氯化铜、硝酸钠中的一种或几种组成的.为确定其成分,向该溶液中逐渐加入氢氧化钡溶液,产生沉淀质量与加入氢氧化钡溶液体积的关系如图所示.
某溶液是由硫酸钠、碳酸钠、盐酸、氯化铜、硝酸钠中的一种或几种组成的.为确定其成分,向该溶液中逐渐加入氢氧化钡溶液,产生沉淀质量与加入氢氧化钡溶液体积的关系如图所示. 某化学兴趣小组的同学为了测定某厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的质量分数不低于99.2%),设计如下两种实验方案:
某化学兴趣小组的同学为了测定某厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的质量分数不低于99.2%),设计如下两种实验方案: