题目内容
11.经测定磁铁矿石比赤铁矿石中含铁量高,所炼出来的铁比较纯净,写出工业上用磁铁矿炼铁的化学方程式Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2,写出常温下能与二氧化碳发生化合反应的一个化学方裎式CO2+H2O═H2CO3.分析 工业上用一氧化碳还原磁铁矿石炼铁,主要是利用CO的还原性,在高温下和磁铁矿石的主要成分四氧化三铁反应生成铁和二氧化碳;常温下水能与二氧化碳发生化合反应生成碳酸,写出反应的化学方程式即可.
解答 解:工业上用一氧化碳还原磁铁矿石炼铁,主要是利用CO的还原性,在高温下和磁铁矿石的主要成分四氧化三铁反应生成铁和二氧化碳,反应的化学方程式为Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
常温下水能与二氧化碳发生化合反应生成碳酸,反应的化学方程式为:CO2+H2O═H2CO3.
故答案为:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;CO2+H2O═H2CO3.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
1.下列图示实验操作中正确的是( )
| A. | 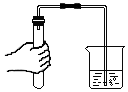 | B. |  | C. | 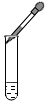 | D. |  |
19.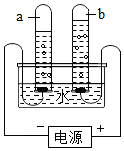 我们的生活离不开水,下列有关水的认识中错误的是( )
我们的生活离不开水,下列有关水的认识中错误的是( )
 我们的生活离不开水,下列有关水的认识中错误的是( )
我们的生活离不开水,下列有关水的认识中错误的是( )| A. | 自然界中的水都是混合物 | |
| B. | 可用肥皂水来区分硬水和软水 | |
| C. | 试管a、b中所得气体的质量比约为2:1 | |
| D. | 试管a、b中所得气体分别为氢气、氧气 |
6.等质量的镁和铝与足量的稀盐酸反应,制得的氢气的质量比是( )
| A. | 2:3 | B. | 1:2 | C. | 1:1 | D. | 3:4 |
3.下列化学反应属于置换反应的是( )
| A. | C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O | B. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | ||
| C. | FeO+CO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2 | D. | Fe+2HCl═FeCl2+H2↑ |
20.如图表示水消毒时所发生的反应的微观过程,下列有关说法正确的是( )


| A. | 图中单质的化学式为O2 | |
| B. | 该反应属于化合反应 | |
| C. | 反应前后分子的个数没变 | |
| D. | 生成物中氯元素的化合价分别为0和+1 |
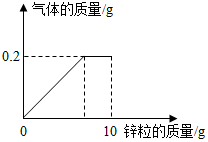 向盛有一定质量稀硫酸的烧杯中逐渐加入10g锌粒,产生气体质量与锌粒质量的关系如图所示,请根据关系图分析并计算:
向盛有一定质量稀硫酸的烧杯中逐渐加入10g锌粒,产生气体质量与锌粒质量的关系如图所示,请根据关系图分析并计算: