题目内容
16.实验室制取气体常用到如图所示装置,根据给出的装置回答下列问题.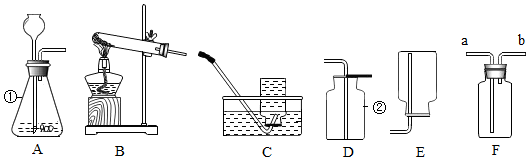
(1)写出标号仪器的名称①锥形瓶;②集气瓶.
(2)若该实验选择装置A来制取氧气,请写出该反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)某同学从上述装置图中选用适当装置成功地制取和收集了二氧化碳.选用的装置是A(填字母).所加药品是碳酸钙和稀盐酸,反应化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
为进一步验证产生的气体是二氧化碳,该同学将气体通入图F装置中,发生反应的方程式是CO2+Ca(OH)2=CaCO3↓+H2O,若在F装置中加入紫色石蕊溶液,观察到的现象是紫色石蕊溶液变红色.
(4)[反思与评价]碳燃烧可以得到二氧化碳,但实验室不用这种方法制二氧化碳,原因是碳燃烧可以生成二氧化碳,不完全燃烧生成一氧化碳,造成该反应的生成的二氧化碳常有一氧化碳杂质.
(5)[表达与交流]气体发生和收集装置的选择依据分别是反应物的状态和反应条件;气体的密度与水溶性.
分析 (1)熟记仪器的名称;
(2)根据实验装置以及化学方程式的写法考虑;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;二氧化碳能够溶于水,密度比空气大,能使澄清石灰水变浑浊;二氧化碳能和水反应生成碳酸,碳酸能使石蕊试液变红色;
(4)根据碳燃烧的产物分析;
(5)根据气体发生装置的选择依据反应物的状态和反应条件;收集气体依据气体的溶解性和密度分析.
解答 解:(1)①是锥形瓶,②是集气瓶;故填:锥形瓶;集气瓶;
(2)该装置适用于固液常温下制取氧气,即过氧化氢制氧气的反应物是过氧化氢,生成物是水和氧气,反应条件是二氧化锰作催化剂,故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)碳酸钙和稀盐酸反应不需要加热,碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,应该用A装置作为发生装置;二氧化碳能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用D装置收集;为了进一步验证产生的气体是二氧化碳,将气体通入F装置中,则F装置中应加入的试剂为Ca(OH)2,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,若在F装置中加入紫色石蕊溶液,观察到的现象是紫色石蕊溶液变红色;故填:A;碳酸钙和稀盐酸;CaCO3+2HCl═CaCl2+H2O+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O;紫色石蕊溶液变红色;
(4)碳燃烧可以生成二氧化碳,不完全燃烧生成一氧化碳,造成该反应的生成的二氧化碳常有一氧化碳杂质,不能用于实验室制取二氧化碳,故填:碳燃烧可以生成二氧化碳,不完全燃烧生成一氧化碳,造成该反应的生成的二氧化碳常有一氧化碳杂质;
(5)根据反应物的状态和反应条件选择发生装置,初中阶段常见的发生装置的特点有:固液常温型和固固加热型两种;收集气体的方法取决于气体的密度与水溶性.
故答案为:反应物的状态和反应条件;气体的密度与水溶性.
点评 本题主要考查仪器的用途、反应表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

 阅读快车系列答案
阅读快车系列答案| 物质 | A | B | C | D |  图例说明 图例说明 |
| 微观示意图 | 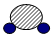 | 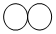 |  |  |
(2)这四种物质中,属于单质的有BC(填表中字母).
(3)常温下A 和B反应生成C和D.请用化学方程式表示此反应:2H2S+O2═2S↓+2H2O(各物质均用化学式表示).
| A. | 2Ca2+-2个钙离子 | B. | H2O-1个水分子 | ||
| C. | O2-2个氧原子 | D. | $\stackrel{0}{{N}_{2}}$-氮气中氮元素的化合价为0 |
| A. | C→CO | B. | CO→CO2 | C. | Fe→FeCl2 | D. | P→P2O5 |
| A. |  液体的加热 | B. |  蒸发溶液 | C. |  液体的取用 液体的取用 | D. |  过滤 |
| A. | 称取的氯化钠固体质量偏大 | |
| B. | 转移配制好的溶液时,有少量液体溅出 | |
| C. | 量取水的体积偏小 | |
| D. | 转移称量好的氯化钠固体时,有少量洒落在桌面 |

