题目内容
7.加热5g氯酸钾和0.3g二氧化锰的混合物,完全反应后得氯化钾3g,同时生成氧气的算式是( )| A. | 5g+0.3g-3g | B. | 5g+3g | C. | 5g-3g | D. | 5g-0.3g-3g |
分析 此题是对质量守恒定律相关应用的考查,由氯酸钾制取氧气的反应可知,二氧化锰作为催化剂,反应前后质量不变,反应前氯酸钾的质量应该等于氯化钾和氧气的质量之和.
解答 解:由氯酸钾制取氧气的反应可知,二氧化锰作为催化剂,反应前后质量不变,反应前氯酸钾的质量应该等于氯化钾和氧气的质量之和.故生成氧气的算式是:5g-3g,
故选C
点评 此题是对质量守恒定律的应用考查,解题的关键是掌握有关催化剂的意义以及相关的化学反应特点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列各物质的变化中,不属于化合反应的是( )
| A. | 生石灰+水→熟石灰 | B. | 甲烷+氧气$\stackrel{点燃}{→}$二氧化碳+水 | ||
| C. | 氧化汞$\stackrel{强热}{→}$氧气+汞 | D. | 铜+氧气→氧化铜 |
15.酸雨的形成主要是由于( )
| A. | 大气中二氧化碳含量的迅速提高 | |
| B. | 工业上大量使用含硫燃料 | |
| C. | 工厂向周围环境排放各种废物、废液 | |
| D. | 农业生产中过量使用有害农药 |
19.有A和B两种物质,在一定条件下反应生成C和D,已知2g A能跟5g B恰好完全反应生成4g C和3g D,现有6g A和20g B,经充分反应后,下列说法中正确的是( )
| A. | 生成C和D的质量之和为26 g | B. | 生成12 g C | ||
| C. | 有1 g A剩余 | D. | 生成10 g D |


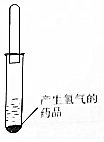 在一次兴趣小组活动中,老师只提供甲同学一大一小两种试管和能产生氢气的化学药品.甲同学设计了如图所示的装置,每次用小试管收集氢气进行验纯时,总是产生尖锐的爆鸣声.请你帮他分析,回答:
在一次兴趣小组活动中,老师只提供甲同学一大一小两种试管和能产生氢气的化学药品.甲同学设计了如图所示的装置,每次用小试管收集氢气进行验纯时,总是产生尖锐的爆鸣声.请你帮他分析,回答: