题目内容
10.请回答下列与金属一个的问题.(1)13g锌与足量的稀硫酸反应,理论上可制得氢气的质量为0.4g.
(2)使用下列各组试剂,能验证Fe、Cu、Ag活动性顺序的是CF.
A.Ag、FeSO4溶液、CuSO4溶液
B.Fe、Cu、AgNO3溶液
C.Fe、Ag、CuSO4溶液
D.Fe、CuSO4溶液、AgNO3溶液
E.Fe、Ag、Cu、稀硫酸
F.Cu、FeSO4溶液、AgNO3溶液.
分析 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,比较简单,计算过程中要注意规范性和准确性.判断金属活动性顺序的基本方法有两种,一是通过金属与酸反应,二是通过金属与盐溶液反应.先根据现象判断是否反应,根据反应情况判断金属活动性,最后进行综合得出结论.
解答 解:(1)设生成氢气的质量为x,
Zn+H2SO4═ZnSO4+H2↑,
65 2
13g x
$\frac{65}{2}=\frac{13g}{x}$ 解得:x=0.4g,
(2)A、银不能与FeSO4溶液、CuSO4溶液,说明Fe、Cu的金属活动性大于银,但不能比较Fe、Cu的活泼性的大小,所以不正确;
B、Fe、Cu都能与AgNO3溶液反应,说明Fe、Cu的金属活动性大于银,但不能比较Fe、Cu的活泼性的大小,所以不正确;
C、铁能置换出硫酸铜中的铜,得出金属活动性铁大于铜,银不能置换出硫酸铜中的铜,得出金属活动性铜大于银,所以正确.
D、Fe和CuSO4溶液、AgNO3溶液均可发生反应,说明Fe>Cu,Fe>Ag.而Cu和Ag无法比较,所以不正确.
E、Fe和稀盐酸反应,得出Fe>H.而Cu和Ag均不能与稀盐酸反应,所以Fe>Cu,Fe>Ag.而Cu和Ag无法比较,所以不正确.
F、铜不能置换出氯化亚铁中的铁,但置换出硝酸银中的银,说明金属活动性是铁大于铜,大于银,所以正确.
故答为:(1)0.4g(2)AB.
点评 掌握金属活动性顺序的判断思路和方法,恰当运用对比的分析方法是解题的前提.

练习册系列答案
相关题目
9. 小聪为了探究燃烧的条件,设计了如图实验装置.通过用力上下振荡锥形瓶可以看到白磷燃烧水火相容的场景,停止振荡则火焰熄灭.该实验直接说明的燃烧需要的条件是( )
小聪为了探究燃烧的条件,设计了如图实验装置.通过用力上下振荡锥形瓶可以看到白磷燃烧水火相容的场景,停止振荡则火焰熄灭.该实验直接说明的燃烧需要的条件是( )
 小聪为了探究燃烧的条件,设计了如图实验装置.通过用力上下振荡锥形瓶可以看到白磷燃烧水火相容的场景,停止振荡则火焰熄灭.该实验直接说明的燃烧需要的条件是( )
小聪为了探究燃烧的条件,设计了如图实验装置.通过用力上下振荡锥形瓶可以看到白磷燃烧水火相容的场景,停止振荡则火焰熄灭.该实验直接说明的燃烧需要的条件是( )| A. | 必须用力上下振荡 | B. | 要有可燃物 | ||
| C. | 温度达到可燃物的着火点 | D. | 与氧气(或空气)接触 |
20.R2+电子数为n,则( )
| A. | 质子数为n+2 | B. | 质子数为n-2 | ||
| C. | 中子数为n+2 | D. | 质子数和中子数都不能确定 |

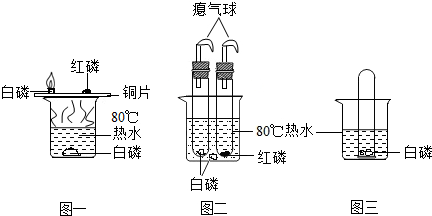
 同学为探究可燃物燃烧的条件,他查阅资料得知:白磷着火点为40℃,红磷着火点为240℃,它们在空气中燃烧都会生成刺激呼吸道的白烟--五氧化二磷,五氧化二磷易溶于水,并能与水反应.他按如图所示装置进行对比实验:
同学为探究可燃物燃烧的条件,他查阅资料得知:白磷着火点为40℃,红磷着火点为240℃,它们在空气中燃烧都会生成刺激呼吸道的白烟--五氧化二磷,五氧化二磷易溶于水,并能与水反应.他按如图所示装置进行对比实验: