题目内容
19.有一包白色固体混和物,可能由Na2SO4、K2CO3、CuSO4、BaCl2、KNO3五种物质中的一种或几种组成.现实验如下:(1)取样品加足量水搅拌,有白色沉淀生成;
(2)过滤得无色滤液;
(3)取沉淀加稀硝酸,沉淀完全溶解,并产生气体.则原固体混和物中一定含有碳酸钾、氯化钡;一定不含有硫酸铜、硫酸钠;可能含有硝酸钾.
分析 根据硫酸铜在溶液中显蓝色,碳酸钾和氯化钡会生成溶于酸的碳酸钡沉淀,硫酸钠和氯化钡生成不溶于酸的硫酸钡沉淀等知识进行分析.
解答 解:硫酸铜在溶液中显蓝色,碳酸钾和氯化钡会生成溶于酸的碳酸钡沉淀,硫酸钠和氯化钡生成不溶于酸的硫酸钡沉淀.
取样品加足量水搅拌,有白色沉淀生成,一定含有氯化钡,可能含有硫酸钠、碳酸钾中的一种或两种;过滤得无色滤液,一定不含硫酸铜;取沉淀加稀硝酸,沉淀完全溶解,并产生气体,一定含有碳酸钾,一定不含硫酸钠,所以原固体混和物中一定含有碳酸钾、氯化钡,一定不含硫酸铜、硫酸钠,可能含有硝酸钾.
故答案为:碳酸钾、氯化钡,硫酸铜、硫酸钠,硝酸钾.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.某化学兴趣小组用火柴、蜡烛、烧杯三种实验材料探究物质燃烧的条件.
【提出问题】物质燃烧需要什么条件?
【猜想与假设】1.有可燃物 2.温度要达到着火点 3.与氧气(或空气)接触
【设计与实验】
【得出结论】猜想正确,燃烧必须同时满足3个条件,只要破坏1个燃烧的条件,就能达到灭火的目的.
【反思质疑 1】氢气在氯气中能燃烧.燃烧是否一定要有氧气参加?
【查阅资料1】镁条能在空气中剧烈燃烧,也能在二氧化碳中剧烈燃烧,发出耀眼的白光、放出大量的热;细铁丝可以在氯气中剧烈燃烧,放出大量的热,产生大量棕黄色的烟;磷能在氯气中剧烈燃烧,放出大量的热,产生大量的白色烟雾.
【表达与交流】根据上述内容和课本中对“燃烧”的描述,你认为发光放热的剧烈的化学反应叫做燃烧.
【反思质疑2】根据“细铁丝在氧气中燃烧”的实验现象,细铁丝在氧气中燃烧为什么会“火星四射”?
【查阅资料2】含碳细铁丝燃烧时,其中的炭粒生成的CO2气体在熔融液态物质中形成气泡,熔融液态物质因气泡炸裂引起“火星四射”的现象.
【设计实验】为了验证细铁丝在纯氧中燃烧产生“火星四射”现象的原因,你设计的实验方案是用用含碳量不同的生铁在氧气中燃烧,比较实验现象.
【提出问题】物质燃烧需要什么条件?
【猜想与假设】1.有可燃物 2.温度要达到着火点 3.与氧气(或空气)接触
【设计与实验】
| 验证 | 对比实验 | |
| 假设1 | 实例:加热烧杯,烧杯不可燃 | ______ |
| 假设2 | 常温放置蜡烛,蜡烛不燃烧 | ______ |
| 假设3 | 点燃蜡烛,蜡烛在空气中持续燃烧 | ______ |
【反思质疑 1】氢气在氯气中能燃烧.燃烧是否一定要有氧气参加?
【查阅资料1】镁条能在空气中剧烈燃烧,也能在二氧化碳中剧烈燃烧,发出耀眼的白光、放出大量的热;细铁丝可以在氯气中剧烈燃烧,放出大量的热,产生大量棕黄色的烟;磷能在氯气中剧烈燃烧,放出大量的热,产生大量的白色烟雾.
【表达与交流】根据上述内容和课本中对“燃烧”的描述,你认为发光放热的剧烈的化学反应叫做燃烧.
【反思质疑2】根据“细铁丝在氧气中燃烧”的实验现象,细铁丝在氧气中燃烧为什么会“火星四射”?
【查阅资料2】含碳细铁丝燃烧时,其中的炭粒生成的CO2气体在熔融液态物质中形成气泡,熔融液态物质因气泡炸裂引起“火星四射”的现象.
【设计实验】为了验证细铁丝在纯氧中燃烧产生“火星四射”现象的原因,你设计的实验方案是用用含碳量不同的生铁在氧气中燃烧,比较实验现象.
14.为了鉴别一桶实验室用的蒸馏水是否被某种酸污染,下列不可采用的方法是( )
| A. | 取样品少许用PH试纸测定样品的pH值 | |
| B. | 取样品滴入酚酞试液观察颜色是否发生变化 | |
| C. | 加入少量金属锌,看是否产生气泡 | |
| D. | 取样品滴入紫色石蕊试液观察颜色变化 |
4.某兴趣小组按图甲装置对“可燃物燃烧的条件”进行探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问.查阅资料得知白磷的着火点是40℃,红磷的着火点是240℃,燃烧产物P2O5是白色固体,会刺激人体呼吸道,P2O5可与空气中水蒸气反应,生成有毒的偏磷酸(HPO3).
【交流与讨论】白烟对人体健康有害,该实验装置必须改进.
【改进与实验】同学们按改进后的图乙装置进行实验.
请你帮助他们将下表补充完整:
(2)改进后的图乙装置与图甲装置比较,优点是防止白磷燃烧生成的五氧化二磷逸散到空气中,造成污染.
(3)图乙装置仍有不足之处,同学们设计了图丙装置,优势是防止有害物质污染空气,调节试管内的气体压强,避免橡皮塞因试管内气体热膨胀而松动.

【交流与讨论】白烟对人体健康有害,该实验装置必须改进.
【改进与实验】同学们按改进后的图乙装置进行实验.
请你帮助他们将下表补充完整:
| 现象 | 解释 |
| ①a试管中白磷燃烧; ②烧杯中的白磷、b试管中红磷没有燃烧. | 烧杯中的白磷、b试管中红磷没有燃烧原因分别是 (1)①热水中白磷没有燃烧的原因是 达到着火点但没有和氧气接触;②b试管中红磷没有燃烧的原因是 和氧气接触但没有达到着火点. |
(3)图乙装置仍有不足之处,同学们设计了图丙装置,优势是防止有害物质污染空气,调节试管内的气体压强,避免橡皮塞因试管内气体热膨胀而松动.

9.下列实验操作能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO2中的CO | 点燃 |
| B | 除去CaO中的CaCO3 | 加水溶解并过滤 |
| C | 区分羊毛与合成纤维 | 点燃,闻气味 |
| D | 区分稀盐酸和稀硫酸 | 滴加紫色石蕊溶液 |
| A. | A | B. | B | C. | C | D. | D |
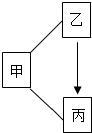 甲、乙、丙是初中化学中常见的物质,其转化关系如图所示(反应条件已省 略).若乙是相对分子质量最小的氧化物,甲、乙均由两种相同的元素组成,请写出实验室由甲制取丙的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
甲、乙、丙是初中化学中常见的物质,其转化关系如图所示(反应条件已省 略).若乙是相对分子质量最小的氧化物,甲、乙均由两种相同的元素组成,请写出实验室由甲制取丙的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑. .
.