题目内容
18.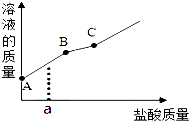 敞口放置的氢氧化钠溶液易吸收空气中的二氧化碳而变质.现向一定质量且部分变质的氢氧化钠溶液中逐滴加入稀盐酸,并振荡.如图表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况.
敞口放置的氢氧化钠溶液易吸收空气中的二氧化碳而变质.现向一定质量且部分变质的氢氧化钠溶液中逐滴加入稀盐酸,并振荡.如图表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况.(1)如图中线段BC对应的实验现象是有气泡产生.
(2)当加入盐酸的质量为a时,溶液中的溶质有NaCl、NaOH、Na2CO3.(写出化学式)
(3)请分析,一定质量的氢氧化钠溶液,变质前后与相同质量分数的稀硫酸反应,变质前消耗硫酸的量=(选填“>”、“=”或“<”)变质后消耗硫酸的量.
分析 氢氧化钠与二氧化碳反应会生成碳酸钠与水,溶液反应时一开始是酸碱中和溶液质量增加,中和完成后会是碳酸钠与盐酸的反应,溶液由于释放出二氧化碳溶液质量增加放缓,至C点反应正好结束,据此分析.
解答 解:(1)从图象可以看出,溶液在AB段质量增加的比BC段要快,所以可以判断AB是中和反应,BC段是盐酸与碳酸钠的反应,这是由于二氧化碳的产生使溶液质量增加放缓,两物质反应的现象是有气泡产生;故答案为:有气泡产生;
(2)当加入盐酸的质量为a时,是盐酸和部分氢氧化钠反应产生氯化钠和水,而碳酸钠没有反应,因此溶质有氯化钠、氢氧化钠和碳酸钠;故答案为:NaCl、NaOH、Na2CO3;
(3)变质前后钠元素质量不变,所以与硫酸充分反应后生成的硫酸钠的质量一定相等,而相等的硫酸钠中硫酸根的质量相同,所以,变质前后所消耗稀硫酸的质量相等;故答案为:=.
点评 此题是一道酸碱盐之间的问题考查题,在对表示反应过程的曲线进行分析时,要注意对曲线起点、折点这些特殊点所表示的意义进行正确分析与判断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.2015年4月6日,位于福建漳州古雷半岛的PX装置发生漏油爆炸;“PX“是对二甲苯的缩写,化学式为C8H10,无色液体,不溶于水,易燃,低毒性化合物.下列说法正确的是( )
| A. | “PX”在氧气中完全燃烧生成二氧化碳和水 | |
| B. | “PX”中碳元素与氢元素质量比为8:10 | |
| C. | “PX”由8个碳原子和10个氢原子构成 | |
| D. | 对二甲苯属于有机高分子化合物 |
9.甲、乙、丙、丁四位同学在实验室里进行如下操作,其中正确的是( )
| A. | 甲做完实验后,将剩余的试剂倒回原试剂瓶 | |
| B. | 丁直接用手将粉末状药品加入试管中 | |
| C. | 丙在取固体粉末时,在无用量说明时取盖满试管底部药品 | |
| D. | 乙在点燃酒精灯时,用燃着的酒精灯引燃另一只酒精灯 |
6.一个碳12原子的实际质量是wg,镁的相对原子质量是24,则一个镁原子的实际质量是( )
| A. | 2g | B. | 12 wg | C. | 12 wg | D. | 2wg |

 将等质量的a、b两种金属粉末分别加入到等质量、等质量分数且足量的稀硫酸中,产生氢气的质量与时间的关系如右图所示.请回答下列问题:(已知a、b两种金属元素在化合物中均为+2价)
将等质量的a、b两种金属粉末分别加入到等质量、等质量分数且足量的稀硫酸中,产生氢气的质量与时间的关系如右图所示.请回答下列问题:(已知a、b两种金属元素在化合物中均为+2价)  如图所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.请回答:
如图所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.请回答: