题目内容
8.用数字和化学符号填空:(1)化学符号表示:
①两个氢氧根离子2OH-.
②用来中和酸性土壤的碱Ca(OH)2.
③氧化镁中镁元素的化合价为+2价$\stackrel{+2}{Mg}$O.
(2)盐酸中能使紫色石蕊溶液变红色的离子是H+,
(2)发酵粉中的盐NaHCO3.
(3)最简单的有机物,是天然气的主要成分CH4.
分析 每个氢氧根离子带1个单位负电荷;
用来中和酸性土壤的碱是氢氧化钙,氢氧化钙中,钙元素的化合价是+2,氢氧根的化合价是-1,根据化合物中元素化合价代数和为零可知,氢氧化钙中钙原子核氢氧根的个数比是1:2;
元素的化合价应该标在元素符号的正上方;
盐酸中能使紫色石蕊溶液变红色的离子是氢离子,每个氢离子带1个单位正电荷;
发酵粉中的盐是碳酸氢钠;
天然气的主要成分是甲烷,每个甲烷分子由1个碳原子和4个氢原子构成.
解答 解:(1)①两个氢氧根离子可以表示为2OH-;
②用来中和酸性土壤的碱是氢氧化钙,可以表示为Ca(OH)2;
③氧化镁中镁元素的化合价为+2价可以表示为$\stackrel{+2}{Mg}$O;
(2)盐酸中能使紫色石蕊溶液变红色的离子是氢离子,可以表示为H+;
(2)发酵粉中的盐是碳酸氢钠,可以表示为NaHCO3;
(3)最简单的有机物是甲烷,可以表示为CH4.
故填:2OH-;Ca(OH)2;$\stackrel{+2}{Mg}$O;H+;NaHCO3;CH4.
点评 本题主要考查学生对化学用语的书写和理解能力,题目重点考查了学生对化学符号的书写,考查全面,注重基础,题目难度较小.

练习册系列答案
相关题目
13. 某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示液,他们对此产生了兴趣.
某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示液,他们对此产生了兴趣.
【提出问题】这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
(1)小明根据标签上的组成元素认为一定不是NaCl;
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是这二者的化学式中Na元素的右下角不会有2;
为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验.
【设计实验】
【实验结论】
(3)该瓶无色溶液是Na2CO3;生成白色沉淀过程的化学方程式是BaCl2+Na2CO3═BaCO3↓+2NaCl.
【实验反思】
(4)小强认为上述设计实验还可简化,仍能达到目的.小强的实验操作是取少量无色溶液样品于试管中,慢慢滴加稀盐酸(合理即可).
 某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示液,他们对此产生了兴趣.
某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示液,他们对此产生了兴趣. 【提出问题】这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
(1)小明根据标签上的组成元素认为一定不是NaCl;
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是这二者的化学式中Na元素的右下角不会有2;
为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验.
【设计实验】
| 实验操作 | 实验现象 |
| 取少量样品于试管中,慢慢滴加BaCl2溶液,静置一段时间,倾去上层清液,向沉淀中继续滴加稀盐酸 | 先出现白色沉淀,后产生大量气泡 |
(3)该瓶无色溶液是Na2CO3;生成白色沉淀过程的化学方程式是BaCl2+Na2CO3═BaCO3↓+2NaCl.
【实验反思】
(4)小强认为上述设计实验还可简化,仍能达到目的.小强的实验操作是取少量无色溶液样品于试管中,慢慢滴加稀盐酸(合理即可).
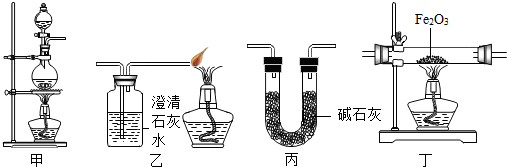
20.某兴趣小组利用以下实验装置模拟工业炼铁的主要过程:
(1)装置甲中发生的反应为:HCOOH ( 甲酸 )$\frac{\underline{\;浓硫酸\;}}{加热}$ CO↑+H2O.
(2)请按合适的顺序连接好以下装置:甲→丙→丁→乙.
(3)丙装置中碱石灰(氧化钙与氢氧化钠混合物)的作用是除去CO中的水蒸气.
(4)丁装置中反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe.
(5)为了探究影响反应产物的外界因素,在Fe2O3与CO反应部位,该小组同学分别用酒精灯和酒精喷灯进行了两次实验,结果如下:
①甲同学猜想黑色产物中可能含有碳单质.乙同学排除了该可能,他提出的两种理由是:碳单质不会被磁铁吸引、CO作还原剂化合价升高不可能生成碳单质.
②丙同学查找资料发现,Fe3O4也能被磁铁吸引,对黑色产物成分提出以下三种假
设:i.全部为铁;ii.全部为四氧化三铁;iii.四氧化三铁和铁的混合物.
③通过进一步定量实验,黑色产物所含元素组成和质量分数如下:
样品Ⅰ的成分及质量分数为w(Fe3O4)=92.8%、w(Fe)=7.2%.

(1)装置甲中发生的反应为:HCOOH ( 甲酸 )$\frac{\underline{\;浓硫酸\;}}{加热}$ CO↑+H2O.
(2)请按合适的顺序连接好以下装置:甲→丙→丁→乙.
(3)丙装置中碱石灰(氧化钙与氢氧化钠混合物)的作用是除去CO中的水蒸气.
(4)丁装置中反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe.
(5)为了探究影响反应产物的外界因素,在Fe2O3与CO反应部位,该小组同学分别用酒精灯和酒精喷灯进行了两次实验,结果如下:
| 加热方式 | 通CO加热时间/min | 澄清石灰水变 浑浊时间/min | 产物颜色 | 产物能否全部 被磁铁吸引 |
| 酒精灯 | 30 | 5 | 黑色 | 能 |
| 酒精喷灯 | 30 | 1 | 黑色 | 能 |
②丙同学查找资料发现,Fe3O4也能被磁铁吸引,对黑色产物成分提出以下三种假
设:i.全部为铁;ii.全部为四氧化三铁;iii.四氧化三铁和铁的混合物.
③通过进一步定量实验,黑色产物所含元素组成和质量分数如下:
| 样品序号 | 加热方式 | 元素组成和质量分数 |
| 产物样品Ⅰ | 酒精灯 | w(Fe)=74.4%、w(O)=25.6% |
| 产物样品Ⅱ | 酒精喷灯 | w(Fe)=100% |
17.学习化学以后,大家学会了从化学的视角观察生活和分析问题.以下说法正确的是( )
| A. | 绿色食品不含任何化学物质 | |
| B. | 胃酸过多的患者可以服用含Al(OH)3的药剂 | |
| C. | 用甲醛溶液作肉类食品的保鲜剂 | |
| D. | “过滤”能将硬水转化成软水 |
18.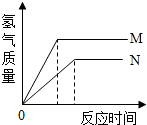 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是( )
等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是( )
 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是( )
等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是( )| A. | M、N两种金属中较活泼的是N | B. | 生成H2的质量M<N | ||
| C. | 相对原子质量较大的是N | D. | 反应消耗等质量的盐酸 |
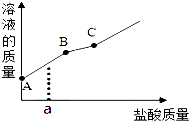 敞口放置的氢氧化钠溶液易吸收空气中的二氧化碳而变质.现向一定质量且部分变质的氢氧化钠溶液中逐滴加入稀盐酸,并振荡.如图表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况.
敞口放置的氢氧化钠溶液易吸收空气中的二氧化碳而变质.现向一定质量且部分变质的氢氧化钠溶液中逐滴加入稀盐酸,并振荡.如图表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况.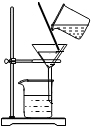 如图是实验室进行过滤操作的装置图,请回答下列问题.
如图是实验室进行过滤操作的装置图,请回答下列问题.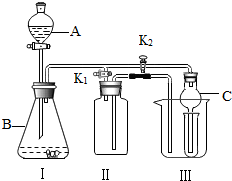 (1)当打开K1关闭K2时,利用Ⅰ、Ⅱ、Ⅲ装置可直接进行的实验时②(填序号)).
(1)当打开K1关闭K2时,利用Ⅰ、Ⅱ、Ⅲ装置可直接进行的实验时②(填序号)).