题目内容
16.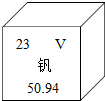 钒被誉为“合金的维生素”,钒元素的相关信息如图所示.下列有关钒的说法不正确的是( )
钒被誉为“合金的维生素”,钒元素的相关信息如图所示.下列有关钒的说法不正确的是( )| A. | 属于金属元素 | B. | 原子序数为23 | ||
| C. | 原子核外电子数为23 | D. | 相对原子质量为50.94g |
分析 由上图该元素在元素周期表中的说明示意图,可得的信息为:原子序数、相对原子质量、核内质子数、核外电子数、元素种类等.
解答 解:A.由的钒汉字名称可得出,钒属于金属元素,故正确;
B.根据元素周期表中钒元素的相关信息:原子序数=核外电子数=质子数=23,故正确;
C.根据元素周期表中钒元素的相关信息:原子序数=核外电子数=质子数=23,故正确;
D.根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,元素的相对原子质量为50.94,相对原子质量单位是“1”,不是“克”,故选项说法错误.
故选:D.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)进行分析解题的能力.

练习册系列答案
相关题目
14.水、食盐、醋、熟石灰均为生活中常见的物质,利用这些物质难以完成的实验是( )
| A. | 鉴别烧碱是否变质 | B. | 柃验自来水中是否含有氯离子 | ||
| C. | 证明鸡蛋壳里含有碳酸盐 | D. | 鉴别白糖和纯碱 |
15.根据实践经验,下列课外实验不能成功的是( )
| A. | 用冷碟子收集蜡烛火焰上方的炭黑 | |
| B. | 用洁净的蛋壳和食醋制得二氧化碳 | |
| C. | 用两杯等体积的水比较报纸与保鲜膜的透气性 | |
| D. | 用自制简易净水器制得纯净水 |
11.南海、钓鱼岛及其附属海域是我国固有领土,蕴藏着丰富的海洋资源.
(1)海水制盐.从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质.为得到较纯的氯化钠,将粗盐溶于水,然后进行如下操作:a.加过量的Ba(OH)2溶液;b.加稍过量的盐酸;c.加过量的Na2CO3溶液;d.过滤;e.蒸发.正确的操作顺序是acdbe(填字母).加Na2CO3溶液的作用是除去氯化钙和过量试剂氢氧化钡.
(2)海水淡化.图1是一个简易的蒸馏法淡化海水的装置.证明得到的水是淡水的最简便方法是蒸干后没有晶体析出.

(3)海水制镁.浓海水中主要离子的浓度如上表.从浓海水中提取金属镁的一段工艺流程如图2所示:
写出反应1的化学方程式:Ca(OH)2+MgCl2=CaCl2+Mg(OH)2↓.滤液X中溶质的主要成分有CaCl2、NaCl(填化学式).将MgCl2溶液在一定条件下蒸发结晶、熔融电解可制得金属镁.则2L浓海水理论上可得到金属镁的质量为57.6g.
(4)海水“制碱”.氨碱法制纯碱是先向饱和食盐水通入氨气、二氧化碳生成NaHCO3和NH4Cl,NaHCO3结晶析出,再加热NaHCO3制得纯碱.写出生成NaHCO3和NH4Cl的化学方程式为NH3+CO2+NaCl+H2O=NaHCO3+NH4Cl;反应中生成NaHCO3和NH4Cl的质量比为84:53.5,NaHCO3和NH4Cl的溶解度曲线如图3所示.请分析NaHCO3结晶析出而NH4Cl没有结晶析出的原因是生成的NaHCO3质量比NH4Cl多而溶解度比NH4Cl小,先达到饱和.
(1)海水制盐.从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质.为得到较纯的氯化钠,将粗盐溶于水,然后进行如下操作:a.加过量的Ba(OH)2溶液;b.加稍过量的盐酸;c.加过量的Na2CO3溶液;d.过滤;e.蒸发.正确的操作顺序是acdbe(填字母).加Na2CO3溶液的作用是除去氯化钙和过量试剂氢氧化钡.
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/g/L | 63.7 | 28.8 | 144.6 | 46.4 |

(3)海水制镁.浓海水中主要离子的浓度如上表.从浓海水中提取金属镁的一段工艺流程如图2所示:
写出反应1的化学方程式:Ca(OH)2+MgCl2=CaCl2+Mg(OH)2↓.滤液X中溶质的主要成分有CaCl2、NaCl(填化学式).将MgCl2溶液在一定条件下蒸发结晶、熔融电解可制得金属镁.则2L浓海水理论上可得到金属镁的质量为57.6g.
(4)海水“制碱”.氨碱法制纯碱是先向饱和食盐水通入氨气、二氧化碳生成NaHCO3和NH4Cl,NaHCO3结晶析出,再加热NaHCO3制得纯碱.写出生成NaHCO3和NH4Cl的化学方程式为NH3+CO2+NaCl+H2O=NaHCO3+NH4Cl;反应中生成NaHCO3和NH4Cl的质量比为84:53.5,NaHCO3和NH4Cl的溶解度曲线如图3所示.请分析NaHCO3结晶析出而NH4Cl没有结晶析出的原因是生成的NaHCO3质量比NH4Cl多而溶解度比NH4Cl小,先达到饱和.
5.下列实验操作错误的是( )
| A. | 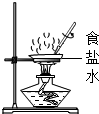 蒸发食盐水 | B. | 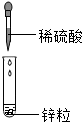 滴管的使用 | ||
| C. | 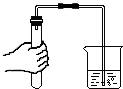 检查装置的气密性 | D. | 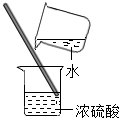 稀释浓硫酸 |
6.下列符号与其叙述对应一致的是( )
| A. | 3H--3个氢元素 | |
| B. | C60--60个碳原子 | |
| C. | ${\stackrel{+3}{AI}}_{\;}$2O3--氧化铝中铝元素的化合价为+3价 | |
| D. | NaCl2--氯化钠 |

