题目内容
11.将H2、N2、CO2、CO、HCl的混合气体依次通入足量的NaOH溶液、碱石灰、灼热的CuO.最后剩下的气体是( )| A. | H2O、N2和CO2 | B. | N2和CO2 | C. | H2O和CO2 | D. | N2 |
分析 根据H2、一氧化碳具有还原性,能与灼热的氧化铜反应,CO2、HCl能与NaOH溶液反应,碱石灰能吸收水分,据此进行分析解答即可.
解答 解:将H2、N2、CO2、CO、HCl的混合气体依次通入足量的NaOH溶液,CO2、HCl能与氢氧化钠溶液反应,CO2、HCl被吸收;碱石灰能吸收水分,通过碱石灰,水蒸气被吸收;H2、一氧化碳具有还原性,通过灼热的CuO,氢气与氧化铜反应生成铜和水蒸气,一氧化碳与氧化铜反应生成生成铜和二氧化碳;故最后剩下的气体是H2O、N2和CO2.
故选:A.
点评 本题难度不大,熟练掌握常见气体的性质是正确解答此类题的关键;解题时要注意在反应中是否生成了新的气体,从而准确判断最后得到的气体.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
5.下列化学用语所表达的意义正确的是( )
| A. | Mg-镁 | B. | 2Na-2个钠元素 | C. | 3Fe2+-3个铁离子 | D. | 4N2-4个氮分子 |
19.要区分下列各组物质,所选择的方法(或试剂)不正确的是( )
| A. | O2和N2--燃着的木条 | B. | 浓硫酸和浓盐酸--扇闻气味 | ||
| C. | 硬水和软水--活性炭 | D. | H2和CO2--澄清石灰水 |
6.下列说法中正确的是( )
| A. | 浓溶液一定是饱和溶液 | |
| B. | 浓硫酸溶解于水时会吸热 | |
| C. | 碘几乎不溶于水,但易溶于酒精 | |
| D. | 100g水中溶解了36gNaCl后达到了饱和,则该氯化钠溶液的质量分数为36% |
20.除去下组内物质中的杂质(括号内物质为杂质),可以用“加适量盐酸、搅拌、过滤、洗涤沉淀、干燥沉淀”的方法的是( )
| A. | CaCO3(Na2CO3) | B. | KCl(MnO2) | C. | NaCl(Na2CO3) | D. | Ag(Al) |
1.有两包白色粉末,它们可能是由AgNO3、BaCl2、K2CO3中的一种或多种物质组成.第一包粉末能溶于稀盐酸,得到澄清溶液,未见其他现象;第二包白色粉末也溶于稀盐酸,产生大量气泡,反应后得到澄清溶液,对上述两包白色粉末成分的结论正确的是( )
| A. | 第一包不含AgNO3、K2CO3,第二包只有K2CO3 | |
| B. | 第一包可能有BaCl2,第二包不含BaCl2 | |
| C. | 第一包肯定是BaCl2,第二包有K2CO3,可能有BaCl2 | |
| D. | 第一包肯定有BaCl2,第二包肯定有K2CO3,不含BaCl2 |
 晓红同学发现她家菜园中的菜生长迟缓,便和爸爸到商店购买氮肥,看到如图是某化肥标签的部分文字,对该化肥的商标所示含氮量产生了怀疑,现请你帮她计算该标签是否属实.
晓红同学发现她家菜园中的菜生长迟缓,便和爸爸到商店购买氮肥,看到如图是某化肥标签的部分文字,对该化肥的商标所示含氮量产生了怀疑,现请你帮她计算该标签是否属实.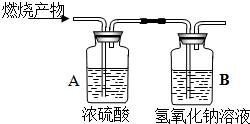 有一钢瓶气体,可能是H2、CO、CH4三种气体中的其中一种或几种的混合,现取少量气体在氧气中燃烧,并将生成的产物通入如图的装置.其中浓硫酸具有吸水性.
有一钢瓶气体,可能是H2、CO、CH4三种气体中的其中一种或几种的混合,现取少量气体在氧气中燃烧,并将生成的产物通入如图的装置.其中浓硫酸具有吸水性.