题目内容
15.请用所学的化学知识解释下列现象(1)NaOH在生活中可用来去除油污,是因为氢氧化钠能与油脂反应.
(2)一氧化碳用于炼铁的原理(用化学方程式表示)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(合理即可).
(3)将一包放置较长时间的食品干燥剂放入烧杯中,加入足量的稀盐酸,可能发生反应的化学方程式有:CaO+2HCl=CaCl2+H2O、Ca(OH)2+2HCl=CaCl2+2H2O、CaCO3+2HCl=CaCl2+H2O+CO2↑;(写三个即可)
分析 (1)氢氧化钠能与油脂反应,据此进行分析解答.
(2)用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳.
(3)氧化钙是常用的食品干燥剂,放置较长时间,能与空气中的水蒸气反应生成氢氧化钙,氢氧化钙能与二氧化碳反应生成碳酸钙和水,一包放置较长时间的食品干燥剂中可能含有氧化钙、氢氧化钙、碳酸钙,据此进行分析解答.
解答 解:(1)氢氧化钠能与油脂反应,在生活中可用来去除油污.
(2)用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(合理即可).
(3)氧化钙是常用的食品干燥剂,放置较长时间,能与空气中的水蒸气反应生成氢氧化钙,氢氧化钙能与二氧化碳反应生成碳酸钙和水,一包放置较长时间的食品干燥剂中可能含有氧化钙、氢氧化钙、碳酸钙,氧化钙与稀盐酸反应生成氯化钙和水、氢氧化钙与盐酸反应生成氯化钙和水、碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式分别为:CaO+2HCl=CaCl2+H2O、Ca(OH)2+2HCl=CaCl2+2H2O、CaCO3+2HCl=CaCl2+H2O+CO2↑.
故答案为:(1)油脂;(2)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(合理即可);(3)CaO+2HCl=CaCl2+H2O、Ca(OH)2+2HCl=CaCl2+2H2O、CaCO3+2HCl=CaCl2+H2O+CO2↑.
点评 本题难度不大,掌握碱的化学性质、氧化钙的化学性质、酸的化学性质、化学方程式的书写方法等是正确解答本题的关键.

| A. | KNO3 NaOH NaNO3 | B. | K2CO3 KCl NaCl | ||
| C. | MgCl2 NaNO3 CuCl2 | D. | Ba(NO3)2 K2SO4 NH4NO3 |
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | 二氧化碳 | 一氧化碳 | 通过适量氢氧化钠溶液 |
| B | 氯化钠溶液 | 氢氧化钠溶液 | 加入适量氯化钡溶液,过滤 |
| C | 氯化钙溶液 | 稀盐酸 | 加入过量碳酸钙,过滤 |
| D | 氯化钾溶液 | 碳酸钾 | 加入过量氯化钙溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
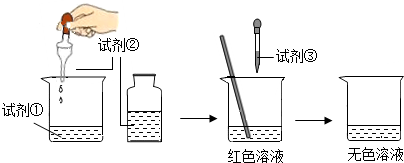
| A. | 稀NaOH溶液、石蕊溶液、稀盐酸 | B. | 稀盐酸、石蕊溶液、稀NaOH溶液 | ||
| C. | 稀NaOH溶液、酚酞溶液、稀盐酸 | D. | 稀盐酸、酚酞溶液、稀NaOH溶液 |
| A. | 石灰石 | B. | 纯碱 | C. | 生石灰 | D. | 熟石灰 |
| A. | KMnO4、K2MnO4 | B. | P2O3、Ca2(PO4)2 | C. | NH4Cl、HNO3 | D. | Cl2、CaCl2 |
 胆矾晶体部分失水后得到某硫酸铜晶体(CuSO4•xH2O),华雪同学为研究CuSO4•xH2O加热后所得物质的组成,做了以下实验:取10.7gCuSO4•xH2O晶体加热使其分解,绘制出固体的质量随温度的变化关系图.(资料:CuSO4•x H2O的相对分子质量为:160+18x)
胆矾晶体部分失水后得到某硫酸铜晶体(CuSO4•xH2O),华雪同学为研究CuSO4•xH2O加热后所得物质的组成,做了以下实验:取10.7gCuSO4•xH2O晶体加热使其分解,绘制出固体的质量随温度的变化关系图.(资料:CuSO4•x H2O的相对分子质量为:160+18x)