题目内容
15.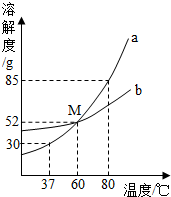 如图为a、b两种物质的溶解度曲线.请根据图中内 容 回答下列问题:
如图为a、b两种物质的溶解度曲线.请根据图中内 容 回答下列问题:(1)随着温度的升高,a物质的溶解度的变化趋势是随着温度升高,a物质的溶解度逐渐增大.
(2)曲线a和b的交叉点M表示的含义是60℃时,a、b两种物质的溶解度相等为52g
(3)37℃时a物质的溶解度比b物质的溶解度小(填“大”或“小”),
37℃时a物质的溶解度为30 g,80℃时40g a物质溶于50g水中所形成的溶液是不饱和溶液(填“饱和”或“不饱和”),溶质质量分数是44.4%.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)溶解度曲线向上倾斜,说明该物质的溶解度随温度的升高而增大.由溶解度曲线图可以看出,随着温度的升高,a物质的溶解度的变化趋势是随着温度升高,a物质的溶解度逐渐增大;
(2)由溶解度曲线图可知,曲线的交点表示该温度下,两种物质的溶解度相同,而且在该温度下两物的饱和溶液中,溶质的质量分数相同.有图象可知,曲线a和b的交叉点M表示的含义是:60℃时,a、b两种物质的溶解度相等为52g;
(3)由溶解度曲线图可知,37℃时a物质的溶解度比b物质的溶解度小,37℃时a物质的溶解度为30g,80℃时a物质的溶解度为85g,所以80℃时40g a物质溶于50g水中所形成的溶液是不饱和溶液,溶质质量分数是:$\frac{40g}{40g+50g}$×100%=44.4%.
故答案为:(1)随着温度升高,a物质的溶解度逐渐增大;
(2)60℃时,a、b两种物质的溶解度相等为52g;
(3)小,30,不饱和,44.4%.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
5.现有两瓶标签脱落的无色溶液,它们分别为石灰水和氢氧化钠溶液,只需选用一种药品就能方便地将它们加以鉴别,该药品是( )
| A. | 紫色石蕊溶液 | B. | 无色酚酞溶液 | C. | 稀盐酸 | D. | 二氧化碳 |
6.同学们应该及时总结归纳学过的知识,某同学总结了以下知识;
①利用金属的化学性质可以区别不同金属的活动性强弱;
②酸、碱中一定含有氢元素;
③能使酸碱指示剂变色的溶液一定是酸溶液或碱溶液;
④糖类、蛋白质都是人体必需的营养素,都属于有机物;
⑤燃烧和缓慢氧化都会放出热量;
⑥用水灭火是因为可降低可燃物的着火点.
其中合理的是( )
①利用金属的化学性质可以区别不同金属的活动性强弱;
②酸、碱中一定含有氢元素;
③能使酸碱指示剂变色的溶液一定是酸溶液或碱溶液;
④糖类、蛋白质都是人体必需的营养素,都属于有机物;
⑤燃烧和缓慢氧化都会放出热量;
⑥用水灭火是因为可降低可燃物的着火点.
其中合理的是( )
| A. | ①②④⑤ | B. | ①③④ | C. | ②⑤⑥ | D. | ②④⑤ |
3. 如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在). 下列说法正确的是( )
如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在). 下列说法正确的是( )
 如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在). 下列说法正确的是( )
如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在). 下列说法正确的是( )| A. | 三种物质的溶解度都随温度的升高而增大 | |
| B. | t2℃时三种物质溶解度大小为:乙>丙>甲 | |
| C. | 将温度由t2℃降到t1℃,所得溶液中溶质的质量分数由大到小的顺序为:乙>甲>丙 | |
| D. | 将温度由t2℃降到t1℃时,析出甲的质量比乙多 |
10.用铁酸钠(Na2FeO4)对来自江湖的淡水进行消毒是城市饮用水处理的新技术,则Na2FeO4中铁元素的化合价为( )
| A. | +2 | B. | +3 | C. | +5 | D. | +6 |
5.将30g铁片放入硫酸铜溶液中片刻后,取出称量铁片质量为31.6g,则参加反应的铁的质量为( )
| A. | 30g | B. | 22.4g | C. | 15g | D. | 11.2g |

 ,离子符号为Mg2+
,离子符号为Mg2+ 写出它的离子符号S2-,该元素的原子核外有3个电子层,它属于非金属元素(“金属”、“非金属”),其化学性质比较活泼,在化学反应中易得到(填“得到”、“失去”)电子.
写出它的离子符号S2-,该元素的原子核外有3个电子层,它属于非金属元素(“金属”、“非金属”),其化学性质比较活泼,在化学反应中易得到(填“得到”、“失去”)电子.

