题目内容
5.将30g铁片放入硫酸铜溶液中片刻后,取出称量铁片质量为31.6g,则参加反应的铁的质量为( )| A. | 30g | B. | 22.4g | C. | 15g | D. | 11.2g |
分析 铁和硫酸铜反应生成硫酸亚铁和铜,根据铁片增加的质量可以计算反应的铁的质量.
解答 解:设参加反应的铁的质量为x,
Fe+CuSO4═FeSO4+Cu,铁片增加的质量
56 64 64-56=8
x 31.6g-30g
$\frac{56}{x}$=$\frac{8}{31.6g-30g}$,
x=11.2g,
故选:D.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.日常生活中的下列变化,一定属于化学变化的是( )
| A. | 爆炸 | B. | 澄清石灰水变浑浊 | ||
| C. | 氢氧化钠固体潮解 | D. | 农家肥的腐熟 |
4.科学中常常出现“1+1≠2”的有趣现象,但也有例外.下列描述符合事实的是( )
| A. | 20℃,1 L水与1 L酒精混合后的体积等于2 L | |
| B. | 20℃,1 g硫粉在1 g氧气中完全燃烧后生成2 g二氧化硫 | |
| C. | 20℃,1 g镁与1 g稀硫酸充分反应后所得的溶液质量为2 g | |
| D. | 20℃,1 g硝酸钾饱和溶液中加入1 g硝酸钾固体能得到2 g硝酸钾溶液 |
1.如图所示图象正确的是( )
| A. | 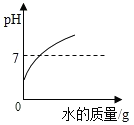 稀释浓硫酸 | |
| B. | 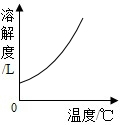 O2的溶解度曲线 | |
| C. | 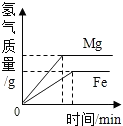 等质量的Mg和Fe与足量同浓度稀盐酸反应 | |
| D. | 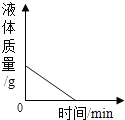 浓硫酸露置空气中 |
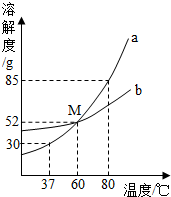 如图为a、b两种物质的溶解度曲线.请根据图中内 容 回答下列问题:
如图为a、b两种物质的溶解度曲线.请根据图中内 容 回答下列问题: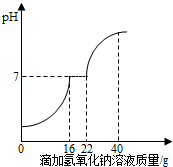 在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说是应为里面含有氯化铁.为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),小霞做了如下实验:取20g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如图所示的关系.
在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说是应为里面含有氯化铁.为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),小霞做了如下实验:取20g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如图所示的关系.