题目内容
通过化学学习,你已经掌握了实验室制取气体的有关规律.图1是某研究性学习小组设计的几种装置,请分析并回答下列问题:
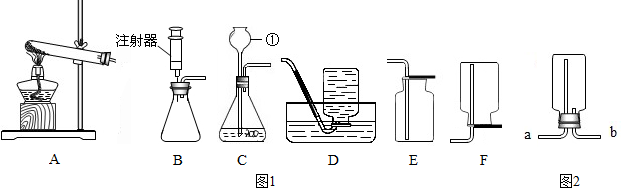
(1)若用氯酸钾和二氧化锰的混合物制取氧气应选用的发生装置为 (填字母).
(2)若用石灰石与稀盐酸混合反应制取二氧化碳气体应选用的发生装置为 (填字母),若要收集二氧化碳可选用的收集装置为 (填字母).实验室制取二氧化碳一般有以下步骤:①检查装置的气密性;②按要求连接制取装置;③向长颈漏斗中注入盐酸;④收集气体;⑤向大试管内放入石灰石,操作顺序正确的是
A.①②③④⑤B.②①③④⑤C.②①⑤③④D.③④⑤②①
(3)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体(化学式为C2H2),该反应必须严格控制加水速度,以免剧烈反应引起发生装置炸裂,你认为图1中最适合制取乙炔气体的发生装置是 (填字母);如图2所示装置收集乙炔气体(化学式为C2H2),气体应从 (填“a”或“b”)端管口通入.
(4)小明采用C装置制取氢气,称取12.5g镁样品,加入足量的稀硫酸,充分反应后,共收集到氢气 1g(假设生成的气体全部收集),试计算该镁样品中镁单质的质量分数.【反应的化学方程式为:Mg+H2SO4 =MgSO4 +H2 ↑ 】

(1)若用氯酸钾和二氧化锰的混合物制取氧气应选用的发生装置为
(2)若用石灰石与稀盐酸混合反应制取二氧化碳气体应选用的发生装置为
A.①②③④⑤B.②①③④⑤C.②①⑤③④D.③④⑤②①
(3)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体(化学式为C2H2),该反应必须严格控制加水速度,以免剧烈反应引起发生装置炸裂,你认为图1中最适合制取乙炔气体的发生装置是
(4)小明采用C装置制取氢气,称取12.5g镁样品,加入足量的稀硫酸,充分反应后,共收集到氢气 1g(假设生成的气体全部收集),试计算该镁样品中镁单质的质量分数.【反应的化学方程式为:Mg+H2SO4 =MgSO4 +H2 ↑ 】
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,制取二氧化碳的操作步骤和注意点,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)根据用氯酸钾和二氧化锰的混合物制取氧气的反应物质的状态及反应条件确定发生装置;
(2)根据用石灰石与稀盐酸混合反应制取二氧化碳的反应物质的状态及反应条件确定发生装置,根据二氧化碳的性质分析收集装置,根据制取二氧化碳的过程和操作分析实验的顺序;
(3)根据实验室在常温下用块状电石与水反应制取乙炔的反应物的状态及反应条件确定发生装置,注射器可以控制加入液体的量;根据乙炔的密度与水的密度的关系分析进气口;
(4)根据镁与盐酸的反应,由氢气的质量求出镁的质量,再求出镁样品中镁单质的质量分数.
(2)根据用石灰石与稀盐酸混合反应制取二氧化碳的反应物质的状态及反应条件确定发生装置,根据二氧化碳的性质分析收集装置,根据制取二氧化碳的过程和操作分析实验的顺序;
(3)根据实验室在常温下用块状电石与水反应制取乙炔的反应物的状态及反应条件确定发生装置,注射器可以控制加入液体的量;根据乙炔的密度与水的密度的关系分析进气口;
(4)根据镁与盐酸的反应,由氢气的质量求出镁的质量,再求出镁样品中镁单质的质量分数.
解答:解:(1)若用氯酸钾和二氧化锰的混合物制取氧气,属于加热固体制取气体,应选用的发生装置为A.
(2)若用石灰石与稀盐酸混合反应制取二氧化碳气体,属于常温下固液反应制取气体,应选用的发生装置为C,由于二氧化碳能溶于水,密度比空气大,若要收集二氧化碳可选用的收集装置为E,实验室制取二氧化碳首先按要求连接制取装置,再检查装置的气密性;固体和液体药品,应先加入固体,再加入液体就可以收集二氧化碳气体.所以C操作正确.
(3)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,属于固液常温下反应制取气体,要控制加水速度,以免剧烈反应放热引起发生装置炸裂,可选择带有注射器的B装置;如右图所示装置收集乙炔气体(化学式为C2H2),由于乙炔的密度小于水的密度,所以,气体应从a端管口通入.
(4)设镁样品中镁单质的质量为X
Mg+H2SO4=MgSO4+H2↑
24 2
X 1克
=
解得:X=12克
镁样品中镁单质的质量分数为:
×100%=96%.
故答为:(1)A;(2)C、E、C;(3)B、a;(4)96%.
(2)若用石灰石与稀盐酸混合反应制取二氧化碳气体,属于常温下固液反应制取气体,应选用的发生装置为C,由于二氧化碳能溶于水,密度比空气大,若要收集二氧化碳可选用的收集装置为E,实验室制取二氧化碳首先按要求连接制取装置,再检查装置的气密性;固体和液体药品,应先加入固体,再加入液体就可以收集二氧化碳气体.所以C操作正确.
(3)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,属于固液常温下反应制取气体,要控制加水速度,以免剧烈反应放热引起发生装置炸裂,可选择带有注射器的B装置;如右图所示装置收集乙炔气体(化学式为C2H2),由于乙炔的密度小于水的密度,所以,气体应从a端管口通入.
(4)设镁样品中镁单质的质量为X
Mg+H2SO4=MgSO4+H2↑
24 2
X 1克
| 24 |
| 2 |
| x |
| 1克 |
镁样品中镁单质的质量分数为:
| 12克 |
| 12.5克 |
故答为:(1)A;(2)C、E、C;(3)B、a;(4)96%.
点评:本道题主要考查了实验室制取气体发生装置和收集装置的选取,发生装置主要由反应物的状态和反应条件决定,收集装置主要由气体的密度和溶水性决定,另外还要考虑气体是否与水反应、是否与空气反应、是否有毒等等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列变化过程中只发生物理变化的是( )
| A、分离液态空气制氧气 |
| B、蜡烛燃烧 |
| C、以大米、高粱、小麦等粮食为原料酿酒 |
| D、铜制品在潮湿的空气中变成铜绿 |
化学用语是学习和交流化学知识的通用语言,以下符号所表达的意义最多的( )
| A、H |
| B、3C60 |
| C、Fe2+ |
| D、Mg |
质量相等的碳酸钙,一份与盐酸反应,另一份高温分解,当完全反应后,两份生成的二氧化碳质量( )
| A、一样多 | B、与盐酸反应生成多 |
| C、加热的多 | D、无法判断 |
 如图是电解水的装置,结合所学知识,完成下列问题:
如图是电解水的装置,结合所学知识,完成下列问题: 实验室一瓶新购进的浓盐酸,其标签的部分内容如图所示,该浓盐酸的溶质是
实验室一瓶新购进的浓盐酸,其标签的部分内容如图所示,该浓盐酸的溶质是