题目内容
10.如图所示为实验室中常见气体制备、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器).试根据题目要求,回答下列问题: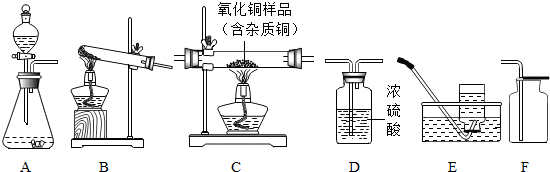
(1)高锰酸钾(KMnO4)固体在加热条件下,能较快地分解为锰酸钾(K2MnO4,可溶固体)、二氧化锰(难溶固体)和氧气.若以高锰酸钾为原料在实验室中制备并收集干燥的氧气:
①所选仪器的连接顺序为BDF(填写仪器序号字母).
②用高锰酸钾制备氧气所发生反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
③从高锰酸钾完全分解后的固体剩余物中提纯锰酸钾的方法是加足量水溶解固体剩余物,过滤,蒸发滤液,使锰酸钾结晶析出
(2)若用锌和稀硫酸反应制取氢气,并用来测定某不纯氧化铜样品的纯度(杂质为少量单质铜),仪器的连接顺序为:A→D1→C→D2→D3(已知:CuO+H2△Cu+H2O;D1、D2、D3为3个浓硫酸洗气瓶).
①仪器C的大玻璃管中可以观察到的现象是黑色粉末变成红色.
②仪器D1的作用是干燥H2,通过测量反应前、后D2浓硫酸洗气瓶的质量变化,来计算氧化铜样品的纯度.若不连接D1,则计算出样品纯度的结果将偏大(填“偏小”“偏大”“不受影响”之一).
③按照正确的仪器连接顺序进行实验,充分反应后测量,仪器D2的质量增加了1.8g,则仪器C大玻璃管内的固体质量应该减少1.6g.
分析 (1)①高锰酸钾制取氧气为固体加热反应,生成的氧气用浓硫酸干燥,用向上排空气法收集;
②据反应原理写出方程式;
③二氧化锰不溶于水,氯化钾溶于水.
(2)根据氢气与氧化铜的反应分析实验的现象;通常情况下,锌和稀硫酸反应生成硫酸锌和氢气;
浓硫酸可以用来干燥氢气;洗气瓶D2的质量增加了1.8g,说明氧化铁和氢气反应生成了1.8g水,1.8g水中氧元素的质量即为C装置内固体减少的质量.
解答 解:(1))①高锰酸钾制取氧气为固体加热反应,生成的氧气用浓硫酸干燥,用向上排空气法收集;
②据反应原理写出方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
③二氧化锰不溶于水,氯化钾溶于水,故加足量水溶解固体剩余物,过滤除去二氧化锰,蒸发滤液,使锰酸钾结晶析出;
(2)①装置C中,在加热的条件下,氢气和氧化铜反应生成了铜和水,反应的现象是:黑色粉末变成红色;
②由于制取的氢气中常含有水蒸气,所以,装置D1的作用是干燥氢气;若不连接D1,生成的氢气中混有的水蒸气,会导致结果偏大;
③充分反应后洗气瓶D2的质量增加了1.8g,则C装置内固体质量减少了:1.8g×$\frac{16}{18}$×100%=1.6g.
故答案为:(1)①B D F ②2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
③加足量水溶解固体剩余物,过滤,蒸发滤液,使锰酸钾结晶析出.(其它合理答案可酌情给分)
(2)①黑色固体变红色 ②干燥H2; 偏大 ③1.6.
点评 理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

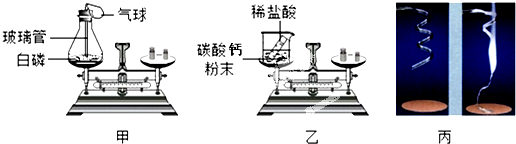
【实验分析】
(1)请你仿照示例,完成实验现象的记录和分析.
| 实验现象 | 化学方程式 | 结论 | |
| 甲同学 | 白磷燃烧产生大量白烟,发光,放热,气球先膨胀后缩小;天平平衡 | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | 该实验遵守质量守恒定律 |
| 乙同学 | 烧杯中有大量气泡产生;天平不平衡. | CaCO3+2HCl=CaCl2+CO2↑+H2O | 该实验遵守质量守恒定律 |
| 丙同学 | 剧烈燃烧、发出耀眼白光、放热 生成 白色固体;反应前后称量质量不相等.(填“相等”或“不相等”) | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | 该实验不遵守质量守恒定律 |
A.氧化物 B.单质 C.混合物
(3)通过对上述实验的对比分析,甲乙两位同学发现丙同学的结论是错误的.在实验操作完全正确的情况下,请分析导致丙同学实验结论错误的原因是反应前未称量参加反应的氧气的质量,反应后生成的氧化镁部分外溢,无法称量.
【实验结论】化学反应都遵守质量守恒定律.
【实验反思】(3)请从微观角度分析化学反应遵守质量守恒定律的原因是化学反应前后原子的种类、数目、质量都没有发生改变.
| A. | 溶液蒸干后,均能得到固体溶质 | |
| B. | 由于缺碘会引起甲状腺肿大,所以我们要多食用加碘食盐 | |
| C. | 物质在溶解得到溶液的过程中,通常有放热或吸热的现象出现 | |
| D. | 糖类、油脂、蛋白质都是由C、H、O三种元素组成的高分子化合物 |
| A. | 多骑自行车,少开汽车 | B. | 大量植树造林 | ||
| C. | 充分利用太阳能 | D. | 直接燃烧煤炭 |
| A. |  加热液体 | B. |  振荡试管 | C. |  放回滴瓶 | D. |  检查气密性 |

