题目内容
11.钢铁是重要的金属材料,在生产、生活中有广泛的用途.建造北京奥运会主体育场“鸟巢”,就是用了大量的钢铁.(1)钢铁的腐蚀给人类来带了巨大的损失.铁在空气中生锈,实际上是铁与空气中的水蒸气和O2(填化学式)共同作用的结果;
(2)日常生活中人们常采用喷漆方法防止钢铁锈蚀;(任意填一种)
(3)在实际生产生活中,还可以利用一定量的酸来除掉铁制品表面的铁锈,请写出利用稀盐酸除铁锈的反应的化学方程式Fe2O3+6HCl=2FeCl3+3H2O.
(4)金属矿物的储量有限,而且不能再生;目前世界上已有50%以上的废钢铁得到回收利用,其目的是节约金属资源.
分析 (1)铁与氧气和水充分接触时容易生锈;
(2)使铁与氧气和水隔绝可以防止生锈;
(3)根据反应物和生成物及其质量守恒定律可以书写化学方程式;
(4)根据金属的回收利用的目的解答,回收金属就是为了节约金属资源.
解答 解:(1)铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果,故填:O2;
(2)在钢铁表面涂漆、镀一层金属等方法可以防止钢铁生锈.故填:喷漆;
(3)用稀盐酸给铁制品除锈的反应是氧化铁和盐酸反应生成氯化铁和水,化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O.故填:Fe2O3+6HCl=2FeCl3+3H2O.
(4)回收利用金属是为了节约金属资源,故填:节约金属资源.
点评 解答本题要充分理解质量守恒定律的内容,同时要理解金属生锈的条件,再根据生锈的条件方面进行分析,从而找出保护金属的方法.

练习册系列答案
相关题目
3.下图中,不属于模型的是( )
| A. |  | B. |  | C. |  | D. |  |

 “防治碘缺乏病日”的主题是“坚持食用碘盐,预防出生缺陷”.据了解,有些偏远地区不少人受到碘缺乏病威胁,这是源于碘盐每500克售价1.2元,不加碘的私盐往往0.5元就卖.巨大的利润驱使不法分子走街串巷,将这些非碘盐直销到偏远地区、农村.
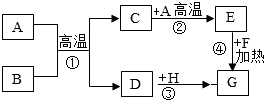
“防治碘缺乏病日”的主题是“坚持食用碘盐,预防出生缺陷”.据了解,有些偏远地区不少人受到碘缺乏病威胁,这是源于碘盐每500克售价1.2元,不加碘的私盐往往0.5元就卖.巨大的利润驱使不法分子走街串巷,将这些非碘盐直销到偏远地区、农村. 物质A、B、C之间有如图所示的转化关系(部分物质和反应条件已经略去).
物质A、B、C之间有如图所示的转化关系(部分物质和反应条件已经略去).