题目内容
2.如图为某同学探究铁、铜、银三种金属活动性顺序的一组实验.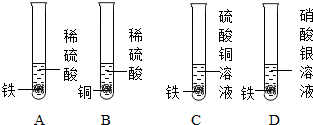
(1)上述实验中,有气泡产生的是A(填字母).
(2)我国古代“湿法冶金”就是利用了C中的反应原理,请写出该反应的实验现象是铁表面产生红色固体,溶液由蓝色变为浅绿色.
(3)通过上述实验,还不能证明铁、铜、银三种金属的金属活动性顺序,请你在此基础上补充一个实验帮助这位同学达到实验目的,写出该实验所需药品的名称铜和AgNO3溶液.
(4)某金属R的样品(杂质不参与反应)10g与73g质量分数为10%的稀盐酸恰好完全反应,生成氢气和金属R的化合物.已知金属R的化合物中氯元素的质量分数为45%,则该样品中R的质量分数为86.8%(计算结果精确到0.1%).
分析 (1)根据铁排在氢的前面能和稀硫酸反应放出氢气,而铜排在氢的后面不能和稀硫酸反应放出氢气进行解答;
(2)根据我国古代“湿法冶铜”的反应原理是铁和硫酸铜反应,铁比铜活泼,可以置换出铜进行解答;
(3)根据ABCD实验可知只能比较出铁比铜活泼和铁比银活泼,但不能验证铜和银的活动性,所以应补充铜和银的盐溶液反应.
(4)据质量守恒定律,化学反应前后元素的种类和质量不变,求出25g 20%的盐酸中氯元素的质量也就是求出生成的盐中氯元素的质量,进而求出生成的盐中R元素的质量,也就是金属R的质量,最后根据R的质量金属样品的质量×100%求出样品中R的质量分数.
解答 解:(1)铁排在氢的前面能和稀硫酸反应放出氢气,而铜排在氢的后面不能和稀硫酸反应放出氢气,上述实验中,有气泡产生的是A;
(2)我国古代“湿法冶铜”的反应原理是铁和硫酸铜反应,铁比铜活泼,可以置换出铜,反应的化学方程式 Fe+CuSO4═FeSO4+Cu;铁表面产生红色固体,溶液由蓝色变为浅绿色;
(3)ABC实验中证明出铁比铜活泼,D试验中证明铁比银活泼,但不能验证铜和银的活动性,应补充铜和银的盐溶液反应.将铜放入到AgNO3溶液中,若铜表面有银白色固体析出,说明铜比银活泼.
(4)氯化氢中氯元素的质量分数为:$\frac{35.5}{36.5}$×100%;
73克20%的稀盐酸中氯元素的质量是:73g×10%×$\frac{35.5}{36.5}$×100%=7.1g;
生成的盐中氯元素的质量分数为45%,则生成的盐中R元素的质量分数也为55%,
生成的盐中R元素的质量为:7.1g×$\frac{55%}{45%}$≈8.68g
那么样品中R的质量分数为:$\frac{8.68g}{10g}$×100%=86.8%
故答案为:
(1)A;
(2)铁表面产生红色固体,溶液由蓝色变为浅绿色;
(3)铜和AgNO3溶液;
(4)86.8%
点评 熟记金属活动性顺序,能判断金属与酸,金属与盐能否反应,根据反应能判断金属的活动性顺序.

 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案实验序号 滴加CuSO4溶液的量 实验现象
①第1-6滴 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液
②第7-9滴 产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色
在实验①中同学们根据所学初中化学知识判断蓝色沉淀是Cu(OH)2,请你写出生成蓝色沉淀的化学方程式2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究.
【查阅资料】Ⅰ.Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO
Ⅱ.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色
【猜想与讨论】小陶认为蓝色沉淀消失可能是Cu(OH)2发生了分解.其他同学一致否定了他的猜测,理由是Cu(OH)2在室温下稳定.
同学们交流讨论后,提出以下两种猜想.
猜想一:少许Cu(OH)2可溶于足量水中.
猜想二:Cu(OH)2可在足量NaOH浓溶液中溶解,溶液呈亮蓝色
【实验探究】为验证猜想,同学们用Cu(OH)2粉末(其它试剂可任选)设计如下实验.请你填写表中的空格.
| 实验序号 | 实验方法与操作 | 实验现象 | 结论 |
| ③ | 将少许Cu(OH)2粉末加到5mL蒸馏水中,充分振荡 | 沉淀不溶解 | 猜想一错误 |
| ④ | 将少许Cu(OH)2粉末加到NaOH浓溶液中,充分振荡 | 沉淀溶解 | 猜想二正确 |
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/ | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
(2)当硝酸钾中混有少量氯化钠时,提纯硝酸钾所采用的方法为降温结晶
(3)将等质量硝酸钾的饱和溶液和氯经钠的饱和溶液从60℃降温到20℃,对所得溶液的叙述正确的是AC(填序号)
A、都是饱和溶液 B、溶剂质量:硝酸钾>氯化钠 C、溶液质量:硝酸钾<氯化钠.
 .
.
 人类的生活和工农业生产都离不开水.
人类的生活和工农业生产都离不开水.