题目内容
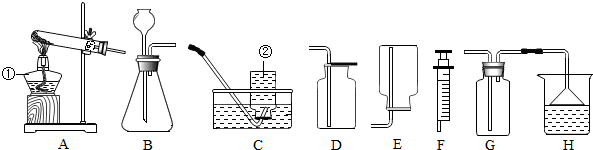
5.实验室配制溶质的质量分数为10%的氯化钠溶液.(1)需要的操作步骤是计算、称量、量取和溶解.
(2)量取蒸馏水要用到的主要仪器是量筒
(3)实际配制的溶液中溶质的质量分数小于10%,其原因可能有ABC.
A.氯化钠固体中含有杂质 B.固体倒入烧杯时洒落 C.配制时烧杯不干燥 D.装瓶时有液体溅出.
分析 (1)在实验室条件下,利用食盐晶体配制溶质质量分数为10%的氯化钠溶液,一般要经过四个步骤:计算所需的溶质质量和溶剂体积;称量和量取所需的溶质和溶剂;把溶质溶解在溶剂中;把配制好的溶液装入试剂瓶中,塞好瓶塞,贴好标签,放入试剂柜中.
(2)在配制溶质的质量分数为10%的氯化钠溶液过程中,我们就要用到相应的实验仪器和药品.称量食盐晶体需要用到托盘天平;量取溶剂离不开量筒;把溶质溶解在溶剂中需要烧杯,并用玻璃棒轻轻搅匀溶液.另外,还要把配制好的溶液装入试剂瓶中,塞好瓶塞,贴好标签,放入试剂柜中.
(3)若溶质质量偏小,将导致溶质质量分数偏小;若溶剂质量偏大也会导致溶质质量分数偏小.据此回答.
解答 解:(1)实验室配制溶质的质量分数为10%的氯化钠溶液,需要的操作步骤是计算、称量、量取和溶解.
(2)量取蒸馏水要用到的主要仪器是量筒.
(3)A.氯化钠固体中含有杂质,造成溶质少了,将导致溶质质量分数偏小;
B.固体倒入烧杯时洒落,造成溶质少了,将导致溶质质量分数偏小;
C.配制时烧杯不干燥,造成溶剂质量偏大,将导致溶质质量分数偏小;
D.装瓶时有液体溅出,溶质质量分数无影响;
所以实际配制的溶液中溶质的质量分数小于10%,其原因可能有ABC.
故答案为:
(1)溶解;
(2)量筒;
(3)ABC.
点评 实验时,一定要了解和认识化学实验室中的各种设备、仪器和药品.本题主要考查分析实验过程的能力,因此正确的分析、解释实验过程是学生应该具备的一种能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列说法错误的是( )
| A. | “酒香不怕巷子深”说明分子是不断运动的 | |
| B. | 分子是保持物质性质的最小粒子 | |
| C. | 原子是化学变化中的最小粒子 | |
| D. | 分子可以化分成原子,原子可以构成分子 |
16.下列化肥中,属于磷肥的是( )
| A. | 过磷酸钙 | B. | 尿素 | C. | 硝酸铵 | D. | 氯化钾 |
20.下列物质的用途中,利用其物理性质的是( )
| A. | 氧气用于炼钢 | B. | 干冰用于人工降雨 | ||
| C. | 硫酸用于处理碱性废液 | D. | 铁粉用作食品保鲜吸氧剂 |
16.请你参与某学习小组研究性学习的过程,并协助完成相关任务.
【研究课题】探究X物质的成分.
【查阅资料】(1)X物质可能由Ca(HCO3)2、Mg(HCO3)2、Ca(OH)2、Mg(OH)2、CaCO3、
BaCO3中的一种或几种组成.
(2)X物质是通过过滤水溶液得到的沉淀.
(3)相关物质的溶解性如下表:
【设计并实施方案】
(1)由查阅资料可知X物质肯定不含可溶性的Ca(HCO3)2、Mg(HCO3)2.
(2)甲同学在烧杯中放入少量研碎的X物质,加入足量蒸馏水充分搅拌,静置.取上层清液滴入Na2CO3溶液,没有白色沉淀,说明X物质中无Ca(OH)2(填化学式).
(3)乙同学设计了下列实验装置,想进一步确定X物质的成分.其主要实验步骤如下:
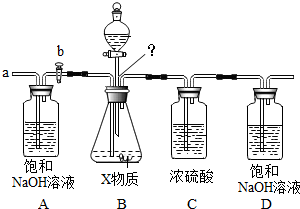
①按图组装仪器,关闭活塞b,将50gX物质的粉末放入锥形瓶中,逐滴加入足量稀硫酸,充分反应.
②待锥形瓶中不再产生气泡时,打开活塞b,从导管a处缓缓鼓入一定量的空气;
③称量D瓶内物质明显增加的质量;
④继续鼓入空气,直至D瓶内物质质量不变;
⑤经称量,D瓶内物质增加的质量为20g.
【评价】(1)A瓶中的NaOH溶液起到吸收鼓入的空气中的二氧化碳作用.若A瓶中无NaOH溶液,D瓶中的质量将增大(填“增大”、“不变”或“减小”).
(2)分析X物质的可能组成是(有几种写几种)Mg(OH)2、CaCO3、BaCO3,或Mg(OH)2、CaCO3或CaCO3、BaCO3.
【研究课题】探究X物质的成分.
【查阅资料】(1)X物质可能由Ca(HCO3)2、Mg(HCO3)2、Ca(OH)2、Mg(OH)2、CaCO3、
BaCO3中的一种或几种组成.
(2)X物质是通过过滤水溶液得到的沉淀.
(3)相关物质的溶解性如下表:
| 物 质 | Ca(HCO3)2 | Mg(HCO3)2 | Ca(OH)2 | Mg(OH)2 | CaCO3 | BaCO3 |
| 溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 不溶 |
(1)由查阅资料可知X物质肯定不含可溶性的Ca(HCO3)2、Mg(HCO3)2.
(2)甲同学在烧杯中放入少量研碎的X物质,加入足量蒸馏水充分搅拌,静置.取上层清液滴入Na2CO3溶液,没有白色沉淀,说明X物质中无Ca(OH)2(填化学式).
(3)乙同学设计了下列实验装置,想进一步确定X物质的成分.其主要实验步骤如下:

①按图组装仪器,关闭活塞b,将50gX物质的粉末放入锥形瓶中,逐滴加入足量稀硫酸,充分反应.
②待锥形瓶中不再产生气泡时,打开活塞b,从导管a处缓缓鼓入一定量的空气;
③称量D瓶内物质明显增加的质量;
④继续鼓入空气,直至D瓶内物质质量不变;
⑤经称量,D瓶内物质增加的质量为20g.
【评价】(1)A瓶中的NaOH溶液起到吸收鼓入的空气中的二氧化碳作用.若A瓶中无NaOH溶液,D瓶中的质量将增大(填“增大”、“不变”或“减小”).
(2)分析X物质的可能组成是(有几种写几种)Mg(OH)2、CaCO3、BaCO3,或Mg(OH)2、CaCO3或CaCO3、BaCO3.
12.下列物质由原子构成的是( )
| A. | 氨气 | B. | 金 | C. | 水 | D. | 硫酸铜 |