题目内容
金属材料在我国建设中起着重要的作用.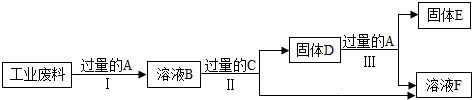
(1)钢铁舰身的锈蚀主要是铁与空气中的 共同作用的结果.
(2)工业上用一氧化碳和赤铁矿炼铁反应的化学方程式为 .
(3)回收利用是保护金属资源的一条有效途径.某工业废料含氧化铜和氧化铁,经过处理后可得到铜和硫酸亚铁溶液,主要流程如图.
已知:CuO+H2SO4═CuSO4+H2O Fe+Fe2(SO4)3═3FeSO4
①过程Ⅰ中氧化铁发生反应的化学方程式是 .
②过程Ⅱ充分反应后,还应有的实验操作是 .
③过程Ⅲ加入适量A,发生反应的化学方程式是 .
④A~F中含铁元素的有 (填序号).

(1)钢铁舰身的锈蚀主要是铁与空气中的
(2)工业上用一氧化碳和赤铁矿炼铁反应的化学方程式为
(3)回收利用是保护金属资源的一条有效途径.某工业废料含氧化铜和氧化铁,经过处理后可得到铜和硫酸亚铁溶液,主要流程如图.
已知:CuO+H2SO4═CuSO4+H2O Fe+Fe2(SO4)3═3FeSO4
①过程Ⅰ中氧化铁发生反应的化学方程式是
②过程Ⅱ充分反应后,还应有的实验操作是
③过程Ⅲ加入适量A,发生反应的化学方程式是
④A~F中含铁元素的有
考点:金属锈蚀的条件及其防护,过滤的原理、方法及其应用,金属的化学性质,铁的冶炼,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)根据铁锈蚀的条件分析回答.
(2)工业上常用一氧化碳和赤铁矿(主要成分为Fe2O3)在高温下反应炼铁,写出反应的化学方程式即可.
(3)氧化铁能与硫酸反应生成硫酸铁和水;分离不溶性固体和液体使用过滤的方法;据此进行解答.
(2)工业上常用一氧化碳和赤铁矿(主要成分为Fe2O3)在高温下反应炼铁,写出反应的化学方程式即可.
(3)氧化铁能与硫酸反应生成硫酸铁和水;分离不溶性固体和液体使用过滤的方法;据此进行解答.
解答:解:(1)钢铁的锈蚀主要是铁与空气中的氧气、水等物质发生化学反应的结果;故填:H2O和O2;
(2)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO
2Fe+3CO2;故填:Fe2O3+3CO
2Fe+3CO2;
(3)①要最终得到硫酸亚铁,则溶解氧化铜和氧化铁使用的酸是稀硫酸,氧化铁能与稀硫酸反应生成硫酸铁和水,故填:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
②过程Ⅱ充分反应后,要得到固体和溶液,需要经过过滤操作;故填:过滤;
③为了将硫酸铜中的铜全部置换出来,需要加入过量的铁,要得到纯铜,需要加入硫酸将过量的铁除去;铁与硫酸反应生成硫酸亚铁和氢气.故填:Fe+H2SO4=FeSO4+H2↑;
④根据分析推断,A中含有硫酸,B中含有硫酸铜和硫酸铁,C是铁,D中含有铁和铜,E是铜,F中含有硫酸亚铁,故填:BCDF.
(2)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO
| ||
| ||
(3)①要最终得到硫酸亚铁,则溶解氧化铜和氧化铁使用的酸是稀硫酸,氧化铁能与稀硫酸反应生成硫酸铁和水,故填:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
②过程Ⅱ充分反应后,要得到固体和溶液,需要经过过滤操作;故填:过滤;
③为了将硫酸铜中的铜全部置换出来,需要加入过量的铁,要得到纯铜,需要加入硫酸将过量的铁除去;铁与硫酸反应生成硫酸亚铁和氢气.故填:Fe+H2SO4=FeSO4+H2↑;
④根据分析推断,A中含有硫酸,B中含有硫酸铜和硫酸铁,C是铁,D中含有铁和铜,E是铜,F中含有硫酸亚铁,故填:BCDF.
点评:本题考查了金属的性质,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
每年5月31日为世界无烟日,吸烟有害健康,烟气中一定含有的有毒气体是( )
| A、O2 |
| B、N2 |
| C、CO2 |
| D、CO |
下列变化属于化学变化的是( )
| A、洗衣服晾干 |
| B、自行车爆胎 |
| C、燃放烟花爆竹 |
| D、冰棒融化 |

