题目内容
20.实验前恰当处理实验用品是保证实验成功的关键,下列处理方法中,不正确的是( )| A. | 用pH试纸测定溶液的酸碱度,需先将试纸用水润湿 | |
| B. | 配制一定质量分数的氯化钠溶液,所用烧杯需要干燥 | |
| C. | 做铁丝与硫酸铜溶液反应实验,铁丝需要用砂纸打磨 | |
| D. | 进行过滤操作,需先将滤纸折成圆锥形后放在漏斗中润湿使之紧贴漏斗内壁 |
分析 A、测定溶液的pH,先用水润湿pH试纸,则相当于稀释了被测液,会引起pH值偏高或偏低;
B、考虑烧杯潮湿会改变溶剂的质量
C、考虑铁在空气中时间长了会生锈用砂纸打磨去除铁锈使金属铁与硫酸铜得以充分接触
D、滤纸不紧贴漏斗内壁会影响过滤速度;
解答 解:A、测定溶液的pH,先用水润湿pH试纸,会使测量结果不准确,操作错误;
B、若烧杯潮湿会增大溶剂的质量是配置的溶液溶质质量分数变小;该操作正确;
C、铁在空气中时间长了会生锈用砂纸打磨去除铁锈使金属铁与硫酸铜得以充分接触;故C操作对;
D、滤纸不紧贴漏斗内壁或留有较多气泡时液体不易流下,会影响过滤速度;故D操作对.
故选A.
点评 本题主要考查了实验操作中的注意事项,了解pH试纸检验溶液的酸碱性的方法,测量前试纸不能用水湿润

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.下列曲线正确的是( )
| A. | 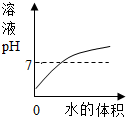 向盐酸中加水 | B. | 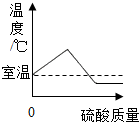 浓H2SO4加入水中 | ||
| C. | 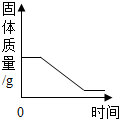 煅烧CaCO3 | D. | 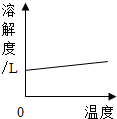 O2在水中的溶解性 |
11.下列一些做法正确的是( )
| A. | 可以用铁桶盛放浓硫酸,但在清洗盛放过浓硫酸的铁桶时,不能遇明火 | |
| B. | 茶壶里的水垢,可以用醋酸或纯碱溶液除去 | |
| C. | 用天平称取NaOH固体时,必须将NaOH固体放在称量纸上 | |
| D. | 除去硫酸铁溶液中混有的硫酸,可以往其中加入铁粉 |
12.实验基本操作是学习化学的灵魂.以下实验操作中正确的是( )
| A. | 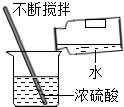 浓硫酸的稀释 | B. | 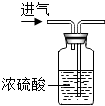 干燥氨气 | C. | 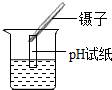 测定某溶液的pH | D. | 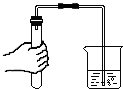 检查气密性 |

 广义的氧化还原反应是指:在反应前后有元素化合价发生变化的化学反应都属于氧化还原反应.如图是小明构建的四种基本反应类型与氧化还原反应的关系图.根据此图回答下列问题:
广义的氧化还原反应是指:在反应前后有元素化合价发生变化的化学反应都属于氧化还原反应.如图是小明构建的四种基本反应类型与氧化还原反应的关系图.根据此图回答下列问题:
