题目内容
10.如图是某同学正在绘制的实验室用高锰酸钾制取氧气的装置图.请回答下列问题: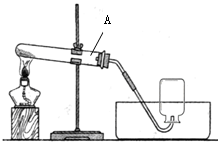
(1)将实验装置图补充完整;
(2)写出用该装置制取氧气的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)在此实验中使用仪器A的注意事项是盛装高锰酸钾的反应容器,用于加热;
(4)收集氧气时,当导管口有气泡连续、均匀的冒出时,再把导管伸入盛满水的集气瓶中.
(5)如果实验结束后,先熄灭酒精灯、后撤导管,会因为反应停止,试管内气体温度降低,气体收缩而导致试管内压强减小,小于外界大气压,在外界大气压的作用下,水槽中的水沿导管到吸入试管底部,致使试管炸裂.
分析 根据加热高锰酸钾制氧气的反应原理,实验装置,实验操作的注意事项进行分析.
实验结束,停止加热时要先把导管移出水面,再熄灭酒精灯,其理由是防止水倒流而炸裂试管;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管.
解答 解:(1)实验室加热高锰酸钾制氧气,盛放高锰酸钾的仪器是试管,试管可以在酒精灯火焰上直接加热;
根据实验室加热高锰酸钾制氧气的装置图进行补充;画图要求:①有棉花;②伸入试管中不能过长;③密封管口,涂黑;④钝角;⑤有胶管,涂黑;⑥弯管口不能超过集气瓶颈部;⑦画出水面实线,中间虚线;
(2)加热高锰酸钾制氧气的方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)仪器A在该实验中的作用是盛装高锰酸钾的反应容器,用于加热;
(4)收集氧气时,当导管口有气泡连续、均匀的冒出时,再把导管伸入盛满水的集气瓶中.
(5)如果实验结束后,先熄灭酒精灯、后撤导管,会因为反应停止,试管内气体温度降低,气体收缩而导致试管内压强减小,小于外界大气压,在外界大气压的作用下,水槽中的水沿导管到吸入试管底部,致使试管炸裂.
故答案为:
(1)
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;(3)盛装高锰酸钾的反应容器,用于加热;(4)导管口有气泡连续、均匀的冒出;(5)压强减小;外界大气压的作用.
点评 熟练掌握实验室制取氧气的反应原理、实验装置及注意事项是解决本题的关键.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
1.某同学在实验室进行有关浓硫酸的实验,观察到瓶上的标签如下表所示.求:
(1)这瓶浓硫酸溶液的质量是多少克?溶质多少克?
(2)若将这瓶浓硫酸与500克水均匀混合,所得稀硫酸的质量分数是多少(结果保留到0.1%)
(3)欲配制1000克质量分数为19.6%的稀硫酸,需要这种浓硫酸多少毫升?水多少毫升?
| 浓硫酸(H2SO4)500毫升 | |
| 溶质的质量分数 | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封储藏 | |
(2)若将这瓶浓硫酸与500克水均匀混合,所得稀硫酸的质量分数是多少(结果保留到0.1%)
(3)欲配制1000克质量分数为19.6%的稀硫酸,需要这种浓硫酸多少毫升?水多少毫升?
18.下列有关氯化钠溶液配制的操作中,正确的是( )
| A. |  称量氯化钠 | B. |  量水的体积 | ||
| C. |  将水倒入烧杯 | D. |  溶解氯化钠时搅拌 |
5.下列化学方程式的书写及其所属基本反应类型均正确的是( )
| A. | 铜在空气中加热表面变黑:Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$ CuO化合反应 | |
| B. | 比较铜和银的活动性:Cu+2AgNO3═2Ag+Cu(NO3)2 置换反应 | |
| C. | 用石灰石与盐酸制取二氧化碳:CaCO3+2HCl═CaCl+H2O+CO2↑分解反应 | |
| D. | 用磁铁矿石(主要成分:Fe3O4)炼铁:4CO+Fe3O4 $\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 还原反应 |
5.下列说法正确的是( )
| A. | 使用催化剂可以生成更多的产物 | |
| B. | 因为水分子中含有氧原子,所以凉开水可以养鱼 | |
| C. | 稀有气体的化学性质不活泼,可作灯泡保护气 | |
| D. | 空气的污染物有可吸入颗粒物、二氧化硫、二氧化碳和二氧化氮等 |
3.与碳元素有关的下列物质中,由原子构成的是( )
| A. | C60 | B. | 石墨 | C. | CO2 | D. | Na2CO3 |
 CuSO4是一种重要的化工原料,电解CuSO4溶液可制得O2等物质,发生的化学反应如下:2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$O2↑+2Cu+2H2SO4,现取一定质量的溶质质量分数为10%的CuSO4溶液进行电解,当CuSO4完全反应时,停止通电,生成O2的质量与时间的关系如图所示,请计算:
CuSO4是一种重要的化工原料,电解CuSO4溶液可制得O2等物质,发生的化学反应如下:2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$O2↑+2Cu+2H2SO4,现取一定质量的溶质质量分数为10%的CuSO4溶液进行电解,当CuSO4完全反应时,停止通电,生成O2的质量与时间的关系如图所示,请计算: