题目内容
20.某铁合金样品1.1g在氧气完全燃烧得到0.013g二氧化碳,通过计算确定该铁合金是生铁还是钢?分析 根据生成的二氧化碳的质量和对应的化学方程式求算样品中碳的含量与标准对比即可(生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%).
解答 解:设样品中碳的质量分数为x
C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2
12 44
1.1gx 0.013g
$\frac{12}{44}$=$\frac{1.1gx}{0.013g}$
x≈0.32%<2%为钢.
答:该铁合金为钢.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.要学好化学,就必须进行化学实验探究.下列因素中与化学实验探究有关的是( )
①提出合理猜想或假设; ②设计探究实验步骤; ③详细记录实验现象和相关数据;
④合作进行化学实验; ⑤形成总结性报告.
①提出合理猜想或假设; ②设计探究实验步骤; ③详细记录实验现象和相关数据;
④合作进行化学实验; ⑤形成总结性报告.
| A. | ①②③④⑤ | B. | ①②③ | C. | ①②③⑤ | D. | ①③⑤ |
8.利用如图装置进行实验.实验前K1、K2、K3均已关闭.
(1)检查装置气密性:保持K1关闭,打开K2、K3,向B中加水至液面浸没下端导管口,用手捂住A瓶外壁,说明装置左侧气密性良好的现象是看到B装置左侧导管口有气泡冒出
(2)实验1中,锌与稀硫酸反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑;气体收集完毕后,在不拆卸装置的情况下,使A中未反应的稀硫酸大部分转移到B中的操作是打开k2,k3,关闭k1.
(3)实验2中,当B中液面不再变化时,B中减少了160mL水,则A中CO2的体积分数约为50%.
| 内容 装置 | 【实验1】制备气体 | 【实验2】测定气体含量 |
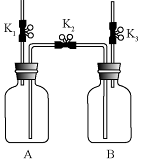 | Ⅰ.打开K1,用注射器向盛有锌粒的A中注入稀硫酸,直至液面浸没下端导管口 Ⅱ.在K1上方导管口收集气体 | Ⅰ.A(容积350ml)中为用排空气法收集的CO2,B中装满水.用注射器向A中注入15mL NaOH溶液(足量),充分反应 Ⅱ.打开K2和K3 |
(2)实验1中,锌与稀硫酸反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑;气体收集完毕后,在不拆卸装置的情况下,使A中未反应的稀硫酸大部分转移到B中的操作是打开k2,k3,关闭k1.
(3)实验2中,当B中液面不再变化时,B中减少了160mL水,则A中CO2的体积分数约为50%.
5.2017年安徽民生热词“舌尖上的安全”.下列做法符合食品安全要求的是( )
| A. | 用亚硝酸钠代替食盐烹调食物 | B. | 用碳酸氢钠作发酵粉 | ||
| C. | 用霉变油菜籽生成食用油 | D. | 用工业酒精勾兑饮用白酒 |
12.如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
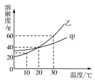

| A. | 通过升温可以将甲的不饱和溶液变为饱和溶液 | |
| B. | 20℃时分别将甲、乙的溶液蒸发相等质量的水,析出甲、乙的质量相等 | |
| C. | 10℃时,10 g水中分别溶解甲、乙达到饱和,溶解较多的物质是乙 | |
| D. | 把100 g溶质质量分数为10%的乙溶液从30℃降温到10℃其质量分数仍为10% |

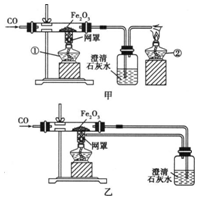 某校课外活动小组的同学在老师的帮助下,探究用赤铁矿(主要成分是Fe2O3)炼铁的主要反应原理.他们设计的实验装置如图所示.回答下列问题:
某校课外活动小组的同学在老师的帮助下,探究用赤铁矿(主要成分是Fe2O3)炼铁的主要反应原理.他们设计的实验装置如图所示.回答下列问题: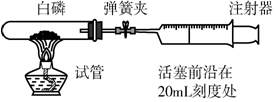 为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为40mL的试管作反应容器,将过量的白磷放入试管,用橡皮塞塞紧试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.假设此实验能够按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:
为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为40mL的试管作反应容器,将过量的白磷放入试管,用橡皮塞塞紧试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.假设此实验能够按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题: