题目内容
6.碘盐就是在食盐中加入一定量的碘酸钾(KIO3),食用碘盐可以有效地预防碘盐缺乏病,(计算结果保留一位小数)请根据化学式计算:(1)KIO3相对分子质量是214;
(2)KIO3中钾、碘、氧元素的质量比为39:127:48.
分析 (1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
解答 解:(1)碘酸钾的相对分子质量=39+127+16×3=214.
(2)碘酸钾中钾元素、碘元素、氧元素的质量比是39:127:(16×3)=39:127:48.
故答案为:(1)214;(2)39:127:48.
点评 本题难度不大,主要考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
17.人类一刻也离不开空气,下列说法不正确的是( )
| A. | 空气是由多种气体组成的混合物 | |
| B. | 空气中的氦气化学性质不活泼,可用于食品防腐 | |
| C. | 空气中的氧气能支持燃烧、供给呼吸 | |
| D. | 空气中的二氧化碳含量增多会引起温室效应,属于空气污染物 |
14.石蜡+氧气$\stackrel{点燃}{→}$水+二氧化碳,则关于石蜡组成的说法中正确的是( )
| A. | 只含碳、氢元素 | |
| B. | 一定含有碳、氧、氢三种元素 | |
| C. | 一定含有碳、氢元素、可能含有氧元素 | |
| D. | 无法确定 |
1.下列有关物质用途的说法中,正确的是( )
| A. | 活性炭可作冰箱除味剂 | B. | 汽油可作油污乳化剂 | ||
| C. | 石灰石可作食品干燥剂 | D. | 氧气可作食品防腐剂 |
18.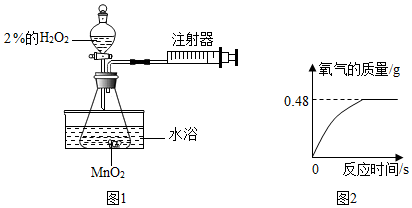 晓晓为了探究温度对H2O2分解速率的影响,利用如图所示装置(夹持装置略去)进行实验(水浴是利用热水进行加热),实验数据记录如表所示:
晓晓为了探究温度对H2O2分解速率的影响,利用如图所示装置(夹持装置略去)进行实验(水浴是利用热水进行加热),实验数据记录如表所示:
(1)实验2中X的值应为40毫升;
(2)实验中,可通过相同的时间内注射器内气体的体积来比较H2O2分解速率的大小;
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因是ac.
a、锥形瓶内气体受热膨胀 b、收集到的氧气中混有空气
c、温度较高时水蒸发成水蒸气 d、生成更多的氧气
(4)晓晓从家中拿来一瓶久置的医用过氧化氢溶液来测定该溶液中溶质质量分数.她取出该溶液51 g,加入适量二氧化锰,生成O2的质量与反应时间的关系如图2所示.
Ⅰ、完全反应后生成氧气的质量为0.015moL.
Ⅱ、计算参与反应的过氧化氢的物质的量0.03mol.(写出计算过程)
Ⅲ、这瓶过氧化氢溶液的质量分数为2%.
 晓晓为了探究温度对H2O2分解速率的影响,利用如图所示装置(夹持装置略去)进行实验(水浴是利用热水进行加热),实验数据记录如表所示:
晓晓为了探究温度对H2O2分解速率的影响,利用如图所示装置(夹持装置略去)进行实验(水浴是利用热水进行加热),实验数据记录如表所示:| 实验1 | 实验2 | |
| MnO2的质量/克 | 0.5 | 0.5 |
| 2%的H2O2的体积/毫升 | 20 | X |
| 温度/℃ | 20 | 80 |
(2)实验中,可通过相同的时间内注射器内气体的体积来比较H2O2分解速率的大小;
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因是ac.
a、锥形瓶内气体受热膨胀 b、收集到的氧气中混有空气
c、温度较高时水蒸发成水蒸气 d、生成更多的氧气
(4)晓晓从家中拿来一瓶久置的医用过氧化氢溶液来测定该溶液中溶质质量分数.她取出该溶液51 g,加入适量二氧化锰,生成O2的质量与反应时间的关系如图2所示.
Ⅰ、完全反应后生成氧气的质量为0.015moL.
Ⅱ、计算参与反应的过氧化氢的物质的量0.03mol.(写出计算过程)
Ⅲ、这瓶过氧化氢溶液的质量分数为2%.
 某实验小组利用如图所示装置探究燃烧条件和研究CO2性质.
某实验小组利用如图所示装置探究燃烧条件和研究CO2性质.