题目内容
17.人类一刻也离不开空气,下列说法不正确的是( )| A. | 空气是由多种气体组成的混合物 | |
| B. | 空气中的氦气化学性质不活泼,可用于食品防腐 | |
| C. | 空气中的氧气能支持燃烧、供给呼吸 | |
| D. | 空气中的二氧化碳含量增多会引起温室效应,属于空气污染物 |
分析 空气中各成分的体积分数分别是:氮气大约占78%、氧气大约占21%、稀有气体大约占0.94%、二氧化碳大约占0.03%、水蒸气和其它气体和杂质大约占0.03%;因此空气是由多种气体组成的混合物;稀有气体是氦、氖、氩、氪、氙等气体的总称,氦气属于稀有气体,稀有气体的用途是:做各种电光源、作保护气等.氧气用途有:支持燃烧和供给呼吸.
解答 解:A、空气中各成分的体积分数分别是:氮气大约占78%、氧气大约占21%、稀有气体大约占0.94%、二氧化碳大约占0.03%、水蒸气和其它气体和杂质大约占0.03%;因此空气是由多种气体组成的混合物,正确但不符合题意,故选项错误;
B、稀有气体是氦、氖、氩、氪、氙等气体的总称,氦气属于稀有气体,稀有气体的用途是:做各种电光源、作保护气等,正确但不符合题意,故选项错误;
C、氧气用途有:支持燃烧和供给呼吸,正确但不符合题意,故选项错误;
D、空气中的二氧化碳含量增多会引起温室效应,但是不属于空气污染物,错误符合题意,故选项正确;
故选D
点评 本考点考查了空气中各种气体的含量和气体的用途等,同学们要加强记忆有关的知识点,在理解的基础上加以应用,本考点基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
16.砒霜是古代很常见的一种毒.由于古代的生产技术落后,致使砒霜里都伴有少量的硫和硫化物.在古代,用银针可以验毒,反应原理是:4Ag+2H2S+O2═2X+2H2O,X的化学式为( )
| A. | Ag2S | B. | Ag2O2 | C. | AgS | D. | Ag2O |
12.硫酸铜溶液对过氧化氢的分解有催化作用,取一定质量8.5%的过氧化氢溶液倒入烧杯中,加入一定质量的硫酸铜溶液,过氧化氢完全分解,有关实验数据如表所示(不考虑气体在水中的溶解),请计算:
(1)生成氧气的质量为0.8g;
(2)所用过氧化氢溶液的质量.
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和过氧化氢溶液的质量/g | 硫酸铜溶液的质量/g | 烧杯和烧杯中溶液的质量/g |
| 50 | 3.3 | 52.5 | |
(2)所用过氧化氢溶液的质量.
2.兰州中科院科研人员研究开发了一套具有超强水净化能力的装置,下列关于水的净化说法不正确的是( )
| A. | 活性炭可除去水中的异味 | B. | 过滤可以除去水中所有的杂质 | ||
| C. | 煮沸可以将硬水软化 | D. | 蒸馏对水的净化程度最高 |
7.学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究.
【猜想】Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2gCuO,取5mL5%过氧化氢溶液于试管中,进行如图实验: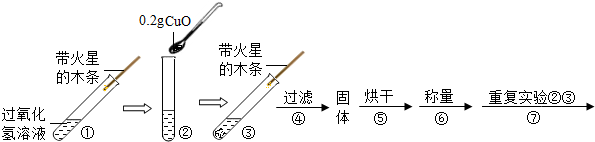
(1)填表:
(2)步骤①的目的是对比实验,比较过氧化氢在有无氧化铜的情况下的分解速率;
步骤⑦的目的是验证氧化铜反应前后额化学性质是否改变;
为了确保实验的严谨与可靠性,步骤⑦中应选用5mL5%的过氧化氢溶液.
(3)步骤④需用到的玻璃仪器有:漏斗、烧杯、玻璃棒.
(4)写出氧化铜加入过氧化氢溶液中所发生的反应的化学方程式2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
【猜想】Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2gCuO,取5mL5%过氧化氢溶液于试管中,进行如图实验:

(1)填表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 无明显现象. | 0.2g | 无明显现象 | 猜想Ⅰ成立 |
| 产生大量气泡,带火星木条复燃. | 不等于0.2g | 产生大量气泡,带火星木条复燃 | 猜想Ⅱ成立 |
| 产生大量气泡,带火星木条复燃 | 0.2g | 产生大量气泡,带火星木条复燃 | 猜想Ⅲ成立 |
步骤⑦的目的是验证氧化铜反应前后额化学性质是否改变;
为了确保实验的严谨与可靠性,步骤⑦中应选用5mL5%的过氧化氢溶液.
(3)步骤④需用到的玻璃仪器有:漏斗、烧杯、玻璃棒.
(4)写出氧化铜加入过氧化氢溶液中所发生的反应的化学方程式2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.


 金属的应用非常广泛,铁是生活中常用的金属.
金属的应用非常广泛,铁是生活中常用的金属.