题目内容
16.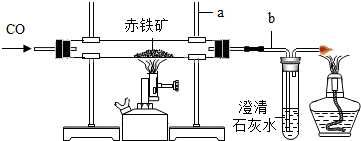 实验室模拟炼铁的实验装置如图所示,赤铁矿的主要成分是氧化铁(Fe2O3).
实验室模拟炼铁的实验装置如图所示,赤铁矿的主要成分是氧化铁(Fe2O3).试回答下列问题:
(1)写出有标号仪器的名称:a铁架台,b导管.
(2)实验中看到的实验现象为:玻璃管中的粉末红色逐渐变成黑色.
(3)玻璃管中反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,氧化剂是Fe2O3.
(4)加热氧化铁之前,先通一会儿一氧化碳的作用是排尽玻璃管中的空气,防止发生爆炸,当反应完全后剩余固体需在CO的保护下冷却其原因是防止铁被重新氧化,防止温度降低压强减小,而导致液体倒吸,造成玻璃管炸裂.
(5)图中酒精灯的作用是除去有毒的一氧化碳气体.
(6)若在模拟实验中通入的气体是H2或CO中的一种,怎样证明通入的气体是CO若澄清的石灰水变浑浊,则证明通入的是CO.
分析 (1)认识常见仪器的名称;
(2)根据实验过程中的实验现象来分析;
(3)在高温的条件下氧化铁被一氧化碳还原为铁,同时产生二氧化碳;
(4)根据可燃性气体不纯加热可能会发生爆炸进行分析解答.防止铁被氧化,石灰水倒吸来分析;
(5)根据一氧化碳有毒,会污染环境,进行分析解答;
(6)根据反应产物来分析.
解答 解:(1)a是铁架台,b是导管;故填:铁架台;导管;
(2)赤铁矿石红色粉末,在高温的条件下被一氧化碳还原为铁,颜色变为黑色;故填:红色逐渐变成黑色;
(3)在高温加热的条件下,一氧化碳能将氧化铁还原为铁,同时生成二氧化碳,其中氧化铁失去氧,发生了还原反应,本身是氧化剂;故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;Fe2O3;
(4)CO具有可燃性,与玻璃管中的空气混合受热会发生爆炸,因此应先通CO排尽玻璃管中的空气,然后再点燃加热氧化铁的酒精灯.当反应完全后剩余固体需在CO的保护下冷却其原因是防止铁被重新氧化,防止温度降低压强减小,而导致液体倒吸,造成玻璃管炸裂;故填:排尽玻璃管中的空气,防止发生爆炸;防止铁被重新氧化,防止温度降低压强减小,而导致液体倒吸,造成玻璃管炸裂.
(5)一氧化碳有毒,直接排放到空气中会污染环境,该实验设计装置酒精灯的目的是燃烧未反应的一氧化碳,防止污染空气.故填:除去有毒的一氧化碳气体;
(6)一氧化碳在高温下还原氧化铁生成二氧化碳,二氧化碳能使澄清的石灰水变浑浊,而氢气的生成物是水,故填:若澄清的石灰水变浑浊,则证明通入的是CO.
点评 本题难度不大,掌握一氧化碳的化学性质(可燃性、还原性等)、还原氧化铁的实验现象等并能灵活运用是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.利用下列物质清洗油污时,发生乳化现象的是( )
| A. | 汽油 | B. | 洗洁精 | C. | 纯碱溶液 | D. | 烧碱溶液 |
7.今有四种粒子的结构示意图,下列说法不正确的是( )
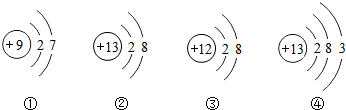

| A. | ④表示的元素在化合物通常显+3价 | |
| B. | 它们表示四种元素 | |
| C. | ①表示的粒子在化学反应中易得到电子 | |
| D. | ②③都表示阳离子 |
11.下列有关金属及合金的说法中正确的是( )
| A. | 铝、铁、铜都是银白色固体,都能导电 | |
| B. | 铜的化学性质不活泼,所以铜制品不会生锈 | |
| C. | 合金是由两种或两种以上金属熔合而成的具有金属特性的物质 | |
| D. | 硬币、不锈钢锅都是合金材料,合金比各成分金属具有更优良的性能 |
6.归纳推理是学习化学的重要方法,以下说法中正确的是( )
| A. | 单质是由同种元素组成的,所以由同种元素组成的物质都是单质 | |
| B. | CO2和CO的组成相同,所以它们的性质也相同 | |
| C. | 原子不显电性,所以构成原子的微粒也都不显电性 | |
| D. | 将燃着的木条伸入集气瓶中,木条熄灭,则集气瓶中的气体可能是二氧化碳 |
 阅读下面科普短文.
阅读下面科普短文.
 甲、乙、丙、丁是常见物质,由氢、碳、氧、氯、钙5种元素中的2~3种组成.
甲、乙、丙、丁是常见物质,由氢、碳、氧、氯、钙5种元素中的2~3种组成.