题目内容
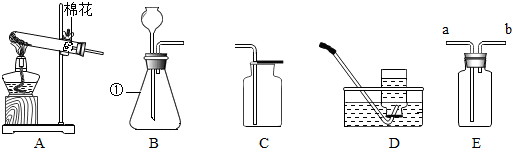
9. 为探究物质的燃烧条件,某同学进行了如图所示的实验.
为探究物质的燃烧条件,某同学进行了如图所示的实验.(1)该实验说明燃烧的条件之一是燃烧需要达到可燃物的着火点.
(2)试验后发现铜片变黑了,质量也变大了,其原因是铜与氧气反应生成了氧化铜;氧化铜的质量包括铜和氧气的质量,故质量增大.
分析 根据已有的知识进行分析,燃烧需要可燃物与氧气接触且温度达到可燃物的着火点;铜能与氧气反应生成氧化铜;据此解答,
解答 解:(1)本题实验中可以观察到乒乓球碎片先燃烧,滤纸片后燃烧,说明燃烧需要达到可燃物的着火点,且乒乓球碎片的着火点比滤纸片的着火点低,故填:燃烧需要达到可燃物的着火点;
(2)在加热的条件下铜能与氧气反应生成氧化铜,氧化铜是黑色的,生成氧化铜的质量包括铜和氧气的质量,故质量增大,故填:铜与氧气反应生成了氧化铜;氧化铜的质量包括铜和氧气的质量,故质量增大;
点评 本题考查了燃烧的条件的实验探究,完成此题,可以依据燃烧的条件进行.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20. 钾是维持人体生命和植物生长所必须的元素.在元素周期表中,钾元素的某些信息如图所示,下列说法不正确的是( )
钾是维持人体生命和植物生长所必须的元素.在元素周期表中,钾元素的某些信息如图所示,下列说法不正确的是( )
 钾是维持人体生命和植物生长所必须的元素.在元素周期表中,钾元素的某些信息如图所示,下列说法不正确的是( )
钾是维持人体生命和植物生长所必须的元素.在元素周期表中,钾元素的某些信息如图所示,下列说法不正确的是( )| A. | 钾元素的符号是K | B. | 钾元素的原子序数为19 | ||
| C. | 钾元素属于非金属元素 | D. | 钾元素的相对原子质量为39.10 |
17.下列生活中常见的变化中,有一个变化与其它三个变化有本质不同,它是( )
| A. | 金桂飘香 | B. | 滴水成冰 | C. | 高粱酿酒 | D. | 彩灯闪烁 |
4.0.8g某物质与氧气反应,生成2.2gCO2和1.8gH2O.下列说法正确的是( )
| A. | 参加反应的O2的质量为3g | B. | 该物质中碳、氢元素质量比为1:4 | ||
| C. | 该物质一定含有碳、氢、氧元素 | D. | 生成CO2和H2O的分子个数比为1:2 |
14.下列变化中,属于物理变化的是( )
| A. | 用分离液态空气法制取氧气 | B. | 用铁矿石冶炼得到生铁 | ||
| C. | 用稀硫酸除铁锈 | D. | 用葡萄来酿制葡萄酒 |
1.下列有关金属及合金的说法中错误的是( )
| A. | 合金的硬度一般比组成它们的纯金属更高,而且耐腐蚀性能更好 | |
| B. | 铜可以与稀硫酸反应生成硫酸铜和氢气 | |
| C. | “真金不怕火炼”说明黄金的化学性质很不活泼 | |
| D. | 大多数金属为电的良导体 |
18. 化学探究课上,老师拿来一瓶标签有破损的试剂瓶,里面盛有一种无色溶液(如图).
化学探究课上,老师拿来一瓶标签有破损的试剂瓶,里面盛有一种无色溶液(如图).
【提出问题】这瓶试剂可能是什么溶液呢?
【做出猜想】第一组:可能是CaO溶液;
第二组:可能是CaCO3溶液;
第三组:可能是CaCl2溶液;
第四组:可能是Ca(OH)2溶液;
第五组:可能是Ca(NO3)2溶液.
【交流讨论】讨论后,大家一致认为第一组和第二组的猜想不正确,
第一组猜想不正确的原因是氧化钙和水反应生成氢氧化钙,无法形成溶液,
第二组猜想不正确的原因是碳酸钙不溶于水,无法形成溶液.
【知识梳理】CaCl2溶液和Ca(NO3)2溶液均为中性,Ca(OH)2溶液为碱性.
【实验探究】
③小美同学认为,X可以是Na2CO3溶液,而小园同学认为X是Na2CO3溶液不能证明第三组猜想成立,理由是(用化学方程式解释)Na2CO3+Ca(NO3)2═2NaNO3+CaCO3↓.
④经大家讨论,一致认为,X应该是AgNO3(填化学式)溶液.
【得出结论】第三组猜想成立,此无色溶液为CaCl2溶液.
 化学探究课上,老师拿来一瓶标签有破损的试剂瓶,里面盛有一种无色溶液(如图).
化学探究课上,老师拿来一瓶标签有破损的试剂瓶,里面盛有一种无色溶液(如图).【提出问题】这瓶试剂可能是什么溶液呢?
【做出猜想】第一组:可能是CaO溶液;
第二组:可能是CaCO3溶液;
第三组:可能是CaCl2溶液;
第四组:可能是Ca(OH)2溶液;
第五组:可能是Ca(NO3)2溶液.
【交流讨论】讨论后,大家一致认为第一组和第二组的猜想不正确,
第一组猜想不正确的原因是氧化钙和水反应生成氢氧化钙,无法形成溶液,
第二组猜想不正确的原因是碳酸钙不溶于水,无法形成溶液.
【知识梳理】CaCl2溶液和Ca(NO3)2溶液均为中性,Ca(OH)2溶液为碱性.
【实验探究】
| 实验方案 | 滴加酚酞溶液 | 通入 ②二氧化碳气体 | 滴加X溶液 |
| 实验操作 | 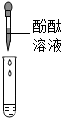 |  | 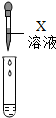 |
| 实验现象 | ①溶液没有变红 | 未出现浑浊 | 产生白色沉 |
| 实验结论 | 第四组猜想不成立 | 第四组猜想不成立 | 第三组猜想成立 |
④经大家讨论,一致认为,X应该是AgNO3(填化学式)溶液.
【得出结论】第三组猜想成立,此无色溶液为CaCl2溶液.