题目内容
4.0.8g某物质与氧气反应,生成2.2gCO2和1.8gH2O.下列说法正确的是( )| A. | 参加反应的O2的质量为3g | B. | 该物质中碳、氢元素质量比为1:4 | ||
| C. | 该物质一定含有碳、氢、氧元素 | D. | 生成CO2和H2O的分子个数比为1:2 |
分析 据质量守恒定律的含义(即六不变)中的“元素的种类不变”可知,生成物所含的碳、氢、氧三种元素中的碳元素和氢元素一定来自于该物质,至于氧元素可能全部来自于氧气,也可能部分来自于氧气,另一部分则来自于该物质,可根据元素的质量不变进行判断;据此分析.
解答 解:根据质量守恒定律可知,该物质一定含有氢元素和碳元素,可能含有氧元素;
二氧化碳中碳元素的质量等于2.2g×$\frac{12}{44}$=0.6g
水中氢元素的质量等于1.8g×$\frac{2}{18}$=0.2g
因此氢元素和碳元素的质量之和是0.6g+0.2g═1.2g=0.8g.说明该物质仅含有碳元素和氢元素,不含氧元素.
A、根据质量守恒定律,参加反应的O2的质量为:2.2g+1.8g-0.8g=3.2g,错误;
B、该物质中碳、氢元素质量比为:0.6:0.2=3:1,错误;
C、该物质仅含有碳元素和氢元素,不含氧元素,错误;
D、生成CO2和H2O的分子个数比为:$\frac{2.2g}{44}:\frac{1.8g}{18}$=1:2,正确.
故选D.
点评 此题是简单的计算题,首先判断物质的组成,然后判断物质的化学式.要求学生掌握判断物质组成的方法.

练习册系列答案
相关题目
14.2016年1月1日我国《环境保护法》颁布一周年,保护环境,人人有责,下列做法不合理的是( )
| A. | 提倡乘坐公交车、骑自行车或步行的出行方式 | |
| B. | 在生产和生活中提倡使用节能技术和节能用具 | |
| C. | 开发新能源,禁止开采和使用化石燃料 | |
| D. | 植树造林,严禁乱砍滥伐 |
15.下列实验操作正确的是( )
| A. | 浓硫酸不小心沾到皮肤上,先用干布拭去,再立刻用稀NaOH溶液冲洗 | |
| B. | 称量氢氧化钠固体时,必须在托盘天平左盘上垫一张洁净白纸 | |
| C. | 测定溶液pH值,将干燥的pH试纸浸入待测溶液片刻后取出,与标准比色卡对比 | |
| D. | 金属钠不慎燃烧不能用水扑灭,应立即用沙子覆盖 |
19.下列图示的实验操作正确的是( )
| A. |  熄灭酒精灯 | B. |  取用碳酸钠固体 | C. | 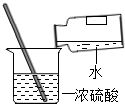 稀释浓硫酸 | D. | 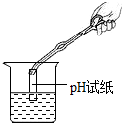 测溶液酸碱度 |
16.下列有关实验现象的描述,错误的是( )
| A. | 木炭在空气中燃烧生成二氧化碳 | |
| B. | 红磷在空气中燃烧,产生大量白烟 | |
| C. | 铁在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 硫在空气中燃烧产生微弱的淡蓝色火焰,并生成有刺激性气味的气体 |
 为探究物质的燃烧条件,某同学进行了如图所示的实验.
为探究物质的燃烧条件,某同学进行了如图所示的实验.