题目内容
18.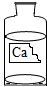 化学探究课上,老师拿来一瓶标签有破损的试剂瓶,里面盛有一种无色溶液(如图).
化学探究课上,老师拿来一瓶标签有破损的试剂瓶,里面盛有一种无色溶液(如图).【提出问题】这瓶试剂可能是什么溶液呢?
【做出猜想】第一组:可能是CaO溶液;
第二组:可能是CaCO3溶液;
第三组:可能是CaCl2溶液;
第四组:可能是Ca(OH)2溶液;
第五组:可能是Ca(NO3)2溶液.
【交流讨论】讨论后,大家一致认为第一组和第二组的猜想不正确,
第一组猜想不正确的原因是氧化钙和水反应生成氢氧化钙,无法形成溶液,
第二组猜想不正确的原因是碳酸钙不溶于水,无法形成溶液.
【知识梳理】CaCl2溶液和Ca(NO3)2溶液均为中性,Ca(OH)2溶液为碱性.
【实验探究】
| 实验方案 | 滴加酚酞溶液 | 通入 ②二氧化碳气体 | 滴加X溶液 |
| 实验操作 | 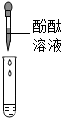 |  | 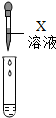 |
| 实验现象 | ①溶液没有变红 | 未出现浑浊 | 产生白色沉 |
| 实验结论 | 第四组猜想不成立 | 第四组猜想不成立 | 第三组猜想成立 |
④经大家讨论,一致认为,X应该是AgNO3(填化学式)溶液.
【得出结论】第三组猜想成立,此无色溶液为CaCl2溶液.
分析 【交流讨论】根据氧化钙和水反应生成氢氧化钙解答;
【知识梳理】根据Ca(OH)2溶液为碱性解答;
【实验探究】
①根据Ca(OH)2溶液为碱性能使无色酚酞溶液变红解答;
②根据Ca(OH)2溶液与二氧化碳反应,产生碳酸钙沉淀解答;
③根据碳酸钠与氯化钙、硝酸钙反应,都产生碳酸钙沉淀解答;
④根据检验氯离子的方法解答.
解答 解:【交流讨论】氧化钙和水反应生成氢氧化钙,无法形成溶液;
【知识梳理】CaCl2溶液和Ca(NO3)2溶液均为中性,Ca(OH)2溶液为碱性;
【实验探究】
①Ca(OH)2溶液为碱性能使无色酚酞溶液变红,往溶液中滴加酚酞溶液,溶液没有变红,说明不是Ca(OH)2溶液,第四组猜想不成立;
②往溶液中通入二氧化碳,未出现浑浊,说明不是Ca(OH)2溶液,第四组猜想不成立;
③小美同学认为,X可以是Na2CO3溶液,而小园同学认为X是Na2CO3溶液不能证明第三组猜想成立,理由是碳酸钠与氯化钙、硝酸钙反应,都产生碳酸钙沉淀,用化学方程式表示为:Na2CO3+Ca(NO3)2═2NaNO3+CaCO3↓;
④硝酸银与氯化钙反应生成氯化银沉淀和硝酸钙,硝酸银与硝酸钙不反应,故X应该是AgNO3溶液;
答案:【交流讨论】氧化钙和水反应生成氢氧化钙,无法形成溶液;
【知识梳理】碱;
【实验探究】
①溶液没有变红;
②二氧化碳;
③Na2CO3+Ca(NO3)2═2NaNO3+CaCO3↓;
④AgNO3.
点评 本题为典型的实验探究中的实验分析题,只有熟练掌握所学知识才能明白实验的设计,才能顺利得出正确答案.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
9.下列关于实验方法的归 纳错误的是( )
| A. | 玻璃仪器一定可以用作反应容器 | |
| B. | 给试管里的固体药品加热时,应先均匀加热,再在固定部位加热 | |
| C. | 取用固体药品可以用药匙、有些块状药品用镊子夹取 | |
| D. | 用过的滴管立即用清水冲洗干净,严禁采用未经清洗的滴管再吸取别的试剂 |
6.下列有关水和溶液的说法正确的是( )
| A. | 自然界中的水都属于化合物,溶液都属于混合物 | |
| B. | 硬水和软水都属于溶液,生活中可通过加热的方法将硬水软化 | |
| C. | 溶液中的溶剂不一定是水,硫酸铜溶液中溶剂是硫酸 | |
| D. | 某物质在100g溶剂里达到饱和状态时所溶解的质量就是该物质的溶解度 |
10.下列做法正确的是( )
| A. | 为了治疗胃酸过多,可以遵循医嘱服用某些碱性的物质,如:氢氧化铝、氢氧化钠 | |
| B. | 工业用盐如亚硝酸钠具有咸味,可以代替食盐用于生活烹调 | |
| C. | 在海水中加入活性炭可以淡化海水 | |
| D. | 在食用皮蛋时可以蘸点食醋,以中和皮蛋中含有的少量碱性物质 |
7.铁铝是生活中常用的金属,下列生活中的一些做法,正确的是( )
| A. | 铁制品的表面生锈后不必立即清除,理由是铁锈能阻止内部的铁继续生锈 | |
| B. | 铝锅用久了表面会有些污垢,最科学的除去污垢的方法是用钢丝球用力擦洗 | |
| C. | 铝制品具有较强的耐腐蚀性,其原因是铝的化学性质不活泼,盛醋最好选择铝制容器 | |
| D. | “暖宝宝”中有铁粉、氯化钠和水等,发热原理是铁粉氧化放热,“暖宝宝”应密封保存 |
8.下列实验现象的描述正确的是( )
| A. | 打开盛有浓盐酸的试剂瓶瓶塞,瓶口有白烟出现 | |
| B. | 硫在空气中燃烧,发出明亮的蓝紫色火焰,生成无色无味的气体 | |
| C. | 向含有酚酞的氢氧化钠溶液中滴加稀盐酸,溶液最终变成无色 | |
| D. | 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 |
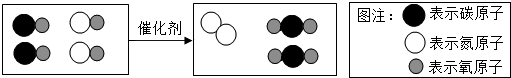
 为探究物质的燃烧条件,某同学进行了如图所示的实验.
为探究物质的燃烧条件,某同学进行了如图所示的实验.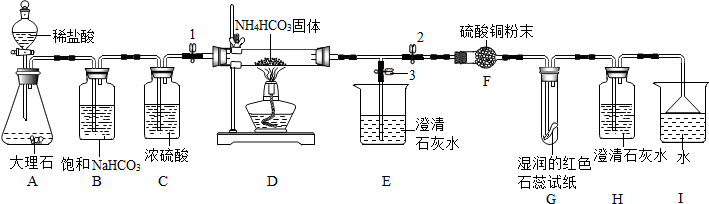
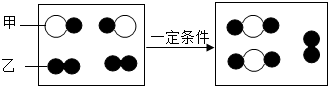
 ”和“
”和“ ”分别表示两种不同的原子.由粒子甲“
”分别表示两种不同的原子.由粒子甲“ ”聚集成的物质可能(填“可能”或“不可能”)是氧化物,参加反应的甲、乙两种反应物分子的个数比为2:1,此反应的基本反应类型为化合反应.任举一例符合此反应类型的化学方程式:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
”聚集成的物质可能(填“可能”或“不可能”)是氧化物,参加反应的甲、乙两种反应物分子的个数比为2:1,此反应的基本反应类型为化合反应.任举一例符合此反应类型的化学方程式:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.