题目内容
11.在实验室中可选择下图装置制取气体.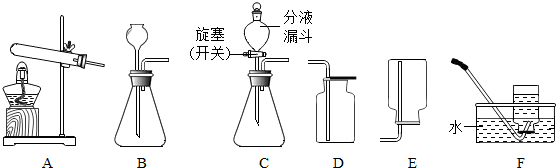
(1)若选择A、F组合一套装置制取了某气体,请写出有关反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(2)制取CO2的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;其发生装置可选择B或C,与B相比较,C的主要优点是可以控制反应的速度.
分析 (1)根据如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.根据装置特点分析解答.
解答 解:
(1)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;C的主要优点是:可以控制反应的速度;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;可以控制反应的速度;
答案:
(1)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑;可以控制反应的速度
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列各组物质间的反应,要借助酸碱指示剂才能判断出反应发生的是( )
| A. | 石灰石与稀盐酸 | B. | 生锈的铁钉与稀盐酸 | ||
| C. | 氧化铜与稀盐酸 | D. | 石灰水与稀盐酸 |
6.以下列举的连云港特产中,主要成分(水除外)属于无机化合物的是( )
| A. | 汪恕有滴醋;主要成分:醋酸 | B. | 汤沟酒;主要成分:乙醇 | ||
| C. | 贝雕;主要成分:碳酸钙 | D. | 葛藤粉;主要成分:淀粉 |
3. 哈尔滨地铁3号线是哈尔滨地铁规划中内城的唯一一条环线.2014 年开始土建施工,2017 年建成开始试运营.下列说法不正确的是( )
哈尔滨地铁3号线是哈尔滨地铁规划中内城的唯一一条环线.2014 年开始土建施工,2017 年建成开始试运营.下列说法不正确的是( )
 哈尔滨地铁3号线是哈尔滨地铁规划中内城的唯一一条环线.2014 年开始土建施工,2017 年建成开始试运营.下列说法不正确的是( )
哈尔滨地铁3号线是哈尔滨地铁规划中内城的唯一一条环线.2014 年开始土建施工,2017 年建成开始试运营.下列说法不正确的是( )| A. | 3号线投入使用后,哈尔滨的市内交通会更加方便、快捷 | |
| B. | 铺设地铁的铁轨,使用的是韧性好、硬度大的不锈钢 | |
| C. | 3号线用B型车辆,铝合金车体.铝是年产量第二高的金属 | |
| D. | 轨道交通由于采用电气牵引,与公共汽车相比不产生废气污染 |
20.汽车安全气囊内的物质能在碰撞后10毫秒内生成空气中体积分数最大的气体,该气体是( )
| A. | 氧气 | B. | 氮气 | C. | 稀有气体 | D. | 二氧化碳 |
1. 某同学用实验的方法检验出甲、乙两种牙膏中都含有碳酸盐并通过实验比较甲、乙牙膏中碳酸钙的质量分数.
某同学用实验的方法检验出甲、乙两种牙膏中都含有碳酸盐并通过实验比较甲、乙牙膏中碳酸钙的质量分数.
【实验原理】通过测定逸出气体的质量,可计算出碳酸钙的质量分数(牙膏中其他物质不与盐酸反应).
【实验步骤】按如图装置进行实验,记录不同时刻装置和药品的总质量,数据如下:
【实验结论】甲牙膏中所含碳酸钙的质量分数大于(填“大于”;“小于”或“等于”)乙牙膏中所含碳酸钙的质量分数.
 某同学用实验的方法检验出甲、乙两种牙膏中都含有碳酸盐并通过实验比较甲、乙牙膏中碳酸钙的质量分数.
某同学用实验的方法检验出甲、乙两种牙膏中都含有碳酸盐并通过实验比较甲、乙牙膏中碳酸钙的质量分数.【实验原理】通过测定逸出气体的质量,可计算出碳酸钙的质量分数(牙膏中其他物质不与盐酸反应).
【实验步骤】按如图装置进行实验,记录不同时刻装置和药品的总质量,数据如下:
| 时间(min) | 0 | 2 | 4 | 6 | 8 | 10 | 12 | |
| 装置和药品总质量(g) | 牙膏甲 | 261.0 | 260.0 | 259.3 | 258.8 | 258.5 | 258.5 | 258.5 |
| 牙膏乙 | 263.0 | 262.4 | 261.9 | 261.4 | 261.0 | 261.0 | 261.0 | |
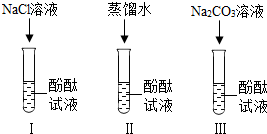 张宁和刘明同学学习完酸、碱、盐后发现:碱溶液能使酚酞溶液变红,Na2CO3溶液也能使酚酞溶液变红.通过学习知道,碱溶液使酚酞溶液变红,是因为碱在水中离解出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞溶液变红呢?请你帮助他俩完成实验探究.
张宁和刘明同学学习完酸、碱、盐后发现:碱溶液能使酚酞溶液变红,Na2CO3溶液也能使酚酞溶液变红.通过学习知道,碱溶液使酚酞溶液变红,是因为碱在水中离解出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞溶液变红呢?请你帮助他俩完成实验探究.