题目内容
1. 张宁和刘明同学学习完酸、碱、盐后发现:碱溶液能使酚酞溶液变红,Na2CO3溶液也能使酚酞溶液变红.通过学习知道,碱溶液使酚酞溶液变红,是因为碱在水中离解出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞溶液变红呢?请你帮助他俩完成实验探究.
张宁和刘明同学学习完酸、碱、盐后发现:碱溶液能使酚酞溶液变红,Na2CO3溶液也能使酚酞溶液变红.通过学习知道,碱溶液使酚酞溶液变红,是因为碱在水中离解出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞溶液变红呢?请你帮助他俩完成实验探究.【提出问题】Na2CO3属于盐(填“酸”、“碱”、“盐”),为什么能使酚酞溶液变红?
【进行猜想】猜想一:Na+使酚酞溶液变红;猜想二:水分子使酚酞溶液变红;猜想三:CO32-使酚酞溶液变红.
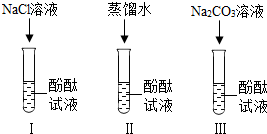
【设计实验】(1)实验Ⅰ的目的是为了验证猜想一不成立.
(2)刘明同学认为实验Ⅱ没必要做,他的理由是酚酞试液中就有水分子(或氯化钠溶液中含有水分子).
(3)实验Ⅲ滴入Na2CO3溶液,振荡,酚酞试液变红.向变红后的溶液中滴加CaCl2溶液至过量,振荡出现的现象是白色沉淀,反应的化学方程式是CaCl2+Na2CO3=CaCO3↓+2NaCl.(提示:CaCl2溶液呈中性)
总结:由实验Ⅰ、Ⅱ、Ⅲ得出猜想三正确.
张宁对此结论有些质疑,于是他查阅资料.
【查阅资料】Na2CO3溶液中,CO32-和H2O发生如下反应:CO32-+H2O=HCO3-+OH-
【得出结论】Na2CO3溶液中使酚酞溶液变红的粒子是OH-.
分析 【提出问题】电离出金属离子和酸根离子的化合物是盐;
【进行猜想】根据碳酸钠溶液中存在的离子分析;
【设计实验】
(1)氯化钠中含有钠离子,可以探究钠离子能否使酚酞变色;
(2)氯化钠溶液中含有大量水分子,所以实验Ⅱ没有必要做;
(3)主要从碳酸钠溶液和氯化钙溶液的反应可以得出,碳酸根离子减少,使红色逐渐消失;碳酸钠和氯化钙反应生成碳酸钙和氯化钠;
【得出结论】氢氧根离子能够使酚酞变红,所以可以判断在碳酸钠溶液中存在氢氧根离子.
解答 解:【提出问题】碳酸钠能电离出钠离子和碳酸根离子,所以属于盐;
【进行猜想】碳酸钠溶液中存在钠离子、碳酸根离子、水分子;
【设计实验】
(1)向氯化钠溶液中加酚酞不变色,说明氯化钠溶液中的粒子都不能使酚酞变红;
(2)氯化钠溶液中含有大量水分子,在实验(1)中得到验证,所以实验(2)的探究是多余的;
(3)碳酸钠溶液和氯化钙溶液反应生成碳酸钙沉淀,所以现象为红色逐渐消失,产生白色沉淀;化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl;
【得出结论】我们知道只有氢氧根离子才能使酚酞变红,所以由碳酸钠溶液能使酚酞溶液变红,可以判断溶液中存在氢氧根离子;
故答案为:【提出问题】盐;
【进行猜想】CO32-
【设计实验】
(1)一;
(2)酚酞试液中就有水分子(或氯化钠溶液中含有水分子);
(3)白色沉淀;
【得出结论】OH-.
点评 本题考查了学生对所提供信息进行处理和利用微粒性质的差异进行实验设计的能力,要求较高.

练习册系列答案
相关题目
12.符合以下四位同学所描述的化学式可能是( )


| A. | H2O | B. | O2 | C. | MgO | D. | HClO |
9.下列物质的用途中,利用其物理性质的是( )
| A. | 天然气作燃料 | B. | 用火碱吸收二氧化硫防治空气污染 | ||
| C. | 铁粉用作食品保鲜吸 | D. | 稀有气体通电会发出有颜色的光 |
16.下列物质鉴别的实验方法错误的是( )
| 鉴别物质 | 实验方法 |
| A过氧化氢和蒸馏水 | 分别加入MnO2,看是否有气泡 |
| B镁和锌 | 分别加入稀盐酸,看是否有气泡 |
| C二氧化碳、氧气和空气 | 将燃着的木条分别伸入瓶中,观察现象 |
| D活性炭和氧化铜 | 分别投入盛有红棕色二氧化氮气体的集气瓶中,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
6.除去下列物质中含有的少量杂质,所用试剂或方法正确的是( )
| 选项 | 物质 | 杂质 | 除杂试剂及操作方法 |
| A | 二氧化碳 | 一氧化碳 | 通入氧气,点燃 |
| B | 氢气 | 氯化氢 | 先 通过过量氢氧化钠溶液,再通过过量浓硫酸 |
| C | 锌粉 | 铁粉 | 加入适量氯化锌溶液,充分反应后过滤 |
| D | 氯化钾溶液 | 碳酸钾 | 加入过量氯化钙溶液,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
10.某同学为了确认某种溶液是否可能为稀盐酸,他取少量这种溶液进行如下实验,其中错误的是( )
| A. | 在取出的溶液中滴入几滴石蕊溶液 | B. | 在取出的溶液中加入石灰石 | ||
| C. | 尝一尝取出溶液是否有酸味 | D. | 在取出的溶液中加入锌粒 |
 眼镜是人们常用的护眼工具,如图是一款变色眼镜的示意图:
眼镜是人们常用的护眼工具,如图是一款变色眼镜的示意图: