题目内容
8.下面是实验室制取氧气的装置图,根据装置图回答下列问题: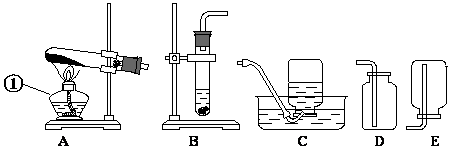
(1)写出装置图中标有①序号的仪器名称:①酒精灯.
(2)实验室用高锰酸钾制取氧气时的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,可选用的发生装置是A;可选用的
收集装置是C或D(写出装置代号).
在实验中试管很容易发生炸裂,分析两条试炸裂管原因:
①试管外壁有水;
②实验后先熄灭酒精灯后撤出导管,导致水槽中冷水倒流炸裂试管.
(3)写出实验室用装置B制取二氧化碳的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
分析 (1)熟记仪器的名称;
(2)根据实验室用氯酸钾制取氧气的反应物的状态以及反应条件选择发生装置;根据氧气的密度和溶解性选择的收集装置;熟记反应原理;
(3)实验室用大理石和稀盐酸反应生成氯化钙、水和二氧化碳,据此书写方程式.
解答 解:(1)仪器①是酒精灯;故填:酒精灯;
(2)实验室用高锰酸钾制取氧气的反应物的状态是固态,反应条件需要加热,所以可选用的发生装置是A;氧气的密度大于空气的密度,所以可选用的收集装置是D;又因为氧气不易溶于水,所以可选用的收集装置还可是C;反应的方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;试管炸裂的原因有:①试管外壁有水,炸裂试管;②实验后先熄灭酒精灯后撤出导管,导致水槽中冷水倒流炸裂试管;③试管加热时没有先均匀预热等;故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;A;C;D;试管外壁有水;实验后先熄灭酒精灯后撤出导管,导致水槽中冷水倒流炸裂试管;
(3)实验室用大理石或石灰石(主要成分是碳酸钙)和稀盐酸反应生成氯化钙、水和二氧化碳,方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑;故填:CaCO3+2HCl═CaCl2+H2O+CO2↑.
点评 本题考查了气体的实验室制法,要熟练掌握反应原理、发生装置的选择、收集装置的选择;另外还要掌握气体的检验、验满及实验操作注意事项等方面的知识,总结实验室制取气体的一般思路和方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.如表是氯化钾和硝酸钾在不同温度时的溶解度.图1是这两种物质的溶解度曲线,图2是相同质量的这两种物质在某温度时分别溶于相同质量的水中的情况.

(1)图1中,t1℃时,b的饱和溶液中溶质与溶液的质量比为1:3.
(2)图2中③、④分别是①、②升温后的情况,则图2中肯定属于饱和溶液的是②(填序号);溶质质量分数变大的是硝酸钾(填物质名称).
(3)图1中t1的温度范围是30℃<t1<40℃.
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | |
| 溶解度(g) | KCl | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |

(1)图1中,t1℃时,b的饱和溶液中溶质与溶液的质量比为1:3.
(2)图2中③、④分别是①、②升温后的情况,则图2中肯定属于饱和溶液的是②(填序号);溶质质量分数变大的是硝酸钾(填物质名称).
(3)图1中t1的温度范围是30℃<t1<40℃.
20.在制取CO2的实验中,小刚发现选用颗粒大小不同的大理石与稀盐酸反应时,CO2的产生速度有差异.经思考后,小刚设计了如图1所示的实验及记录表.请你完成下列问题:
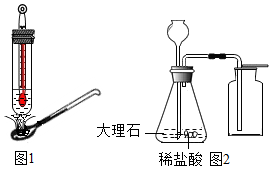
(1)实验①②探究的是大理石和稀盐酸的反应速度与颗粒大小的关系.
(2)探究大理石和稀盐酸的反应速度与稀盐酸质量分数的关系,应选择的实验组是②③.
(3)如图2所示,如要检验该集气瓶是否已收集满CO2,你的方法是把燃着的木条放在集气瓶口,木条熄灭,证明集满.
(4)如要判断实验中产生的CO2速度,最后一列需填写收集满一瓶CO2所需要的时间.
| 实验 序号 | 温 度 (℃) | 大 理 石 | 稀 盐 酸 | |||
| 质量(g) | 颗 粒 | 体积(ml) | 质量分数(%) | |||
| ① | 20 | 5 | 大 | 20 | 5 | |
| ② | 20 | 5 | 小 | 20 | 5 | |
| ③ | 20 | 5 | 小 | 20 | 10 | |

(1)实验①②探究的是大理石和稀盐酸的反应速度与颗粒大小的关系.
(2)探究大理石和稀盐酸的反应速度与稀盐酸质量分数的关系,应选择的实验组是②③.
(3)如图2所示,如要检验该集气瓶是否已收集满CO2,你的方法是把燃着的木条放在集气瓶口,木条熄灭,证明集满.
(4)如要判断实验中产生的CO2速度,最后一列需填写收集满一瓶CO2所需要的时间.
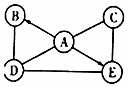 A、B、C、D、E是初中化学常见的五种不同类别的物质.其中B的固体可用于人工降雨,C的组成元素在地壳中含量居第四位,D常用于清洗油污.图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略).请回答下列问题.
A、B、C、D、E是初中化学常见的五种不同类别的物质.其中B的固体可用于人工降雨,C的组成元素在地壳中含量居第四位,D常用于清洗油污.图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略).请回答下列问题.

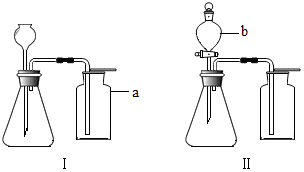 如图是气体制备的装置图.
如图是气体制备的装置图.