题目内容
17.天津海水资源丰富,海水资源利用有良好的发展前景.(1)海水经过蒸发结晶可获得粗盐.
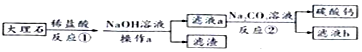
(2)粗盐中含有硫酸镁、氯化钙等可溶性杂质.将粗盐溶于水再进行如下操作:①加过量的Na2CO3溶液;②加过量的Ba(OH)2溶液;③加适量的盐酸;④过滤;⑤蒸发,可得到较纯净的氯化钠.正确的操作顺序为②①④③⑤(用序号填写).蒸发过程中为防止固体飞溅,应采取的措施是用玻璃棒不断搅拌.
(3)用提纯得到的食盐配制50g 5%的NaCl溶液.需用到的玻璃仪器有量筒、玻璃棒、烧杯和胶头滴管.经检测,配好的溶液溶质质量分数偏小,分析原因可能有CD.
A.量取水时,俯视读数B.装瓶时,有少量溶液洒出
C.提纯时得到的晶体仍不纯 D.称量时,砝码端没垫相同的纸片.
分析 (1)根据食盐的溶解度受温度影响变化不大,进行分析解答.
(2)根据镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀,最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子,进行分析解答.
(3)配制50g 5%的NaCl溶液的操作步骤分别是:计算、称量、溶解,确定各操作所需要使用的仪器即可.
溶质质量分数变小,则可能是溶质质量偏小或溶剂质量偏大,可以分析出可能造成这两个方面错误的原因进行分析解答.
解答 解:(1)食盐的溶解度受温度的影响小,从食盐溶液中获得食盐主要利用阳光和风蒸发水分,使海水中的水分蒸发掉,使氯化钠结晶出来.
(2)镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可溶液以将镁离子沉淀;硫酸根离子用钡离子沉淀;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钠溶液转化为沉淀,但是加入碳酸钠溶液要放在加入的过量的Ba(OH)2溶液之后,这样碳酸钠会除去反应剩余的Ba(OH)2;完全反应后,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,所以正确的顺序为:②①④③⑤.
蒸发过程中为防止固体飞溅,应采取的措施是用玻璃棒不断搅拌.
(3)配制50g 5%的NaCl溶液的操作步骤分别是:计算、称量、溶解,在这些操作中需要的仪器:托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒,其中属于玻璃仪器的是玻璃棒、烧杯、胶头滴管、量筒.
A.量取水时,俯视读数,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大.
B.溶液具有均一性,装瓶时有少量溶液洒出,溶质质量分数不变.
C.提纯时得到的晶体仍不纯,会导致称量的氯化钠的质量偏小,则使溶质质量分数偏小.
D.称量时,砝码端没垫相同的纸片,氯化钠和纸片的质量等于砝码和游码的质量,会造成实际所取的溶质的质量偏小,则使溶质质量分数偏小.
故答案为:(1)蒸发;(2)②①④③⑤;用玻璃棒不断搅拌;(3)量筒;CD.
点评 本题难度不大,掌握粗盐提纯的实验原理、盐的化学性质、一定溶质质量分数溶液的配制的步骤(计算、称量、溶解)、注意事项等是正确解答本题的关键.

| A. | 能电离出氢离子的化合物不一定是酸 | |
| B. | 凡是酸的组成中都含有氢和氧元素 | |
| C. | 只由金属离子和酸根离子组成的化合物才是盐 | |
| D. | 凡是能电离出氢氧根离子的化合物都是碱 |
| A. | 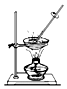 蒸发溶液 | B. |  给液体加热 | ||
| C. |  氢气验纯 | D. | 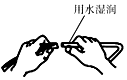 玻璃管和胶皮管连接 |
| A. | 叶绿素是一种含有金属元素的有机混合物 | |
| B. | 叶绿素中氢元素的质量分数最低 | |
| C. | 一个叶绿素分子是由碳氢镁氮氧五种元素构成的 | |
| D. | 叶绿素中碳氧元素的质量比为55:8 |